Caso Clínico #10
O caso clínico abaixo é apresentado em partes. O negrito é a descrição do caso, as partes que não estão em negrito são os comentários. Ao final, você encontrará a resolução e os pontos de aprendizagem resumidos.
Um homem de 38 anos procura atendimento por dispneia iniciada há dois meses, ocorrendo ao realizar tarefas habituais. Os sintomas têm caráter progressivo, resultando em limitação para caminhar uma quadra. Informa também tosse e sudorese noturna, ortopneia, perda de peso de cerca de 8 kg, aumento do volume abdominal e edema de membros inferiores. Nega antecedentes patológicos ou uso de medicamentos.
Ao exame, os sinais vitais eram: pressão arterial 110/70 mmHg, frequência cardíaca de 96 bpm, frequência respiratória de 18 irpm, saturação de 97%, afebril. Havia icterícia 1+/4+ e palidez 1+/4+, além de turgência jugular com refluxo abdominojugular. Foram auscultadas crepitações finas em ambas as bases pulmonares, sopro sistólico panfocal, com maior intensidade em foco mitral, 3+/6+, e presença de B3. Foi observado edema 2+/4+ em membros inferiores, simétrico.
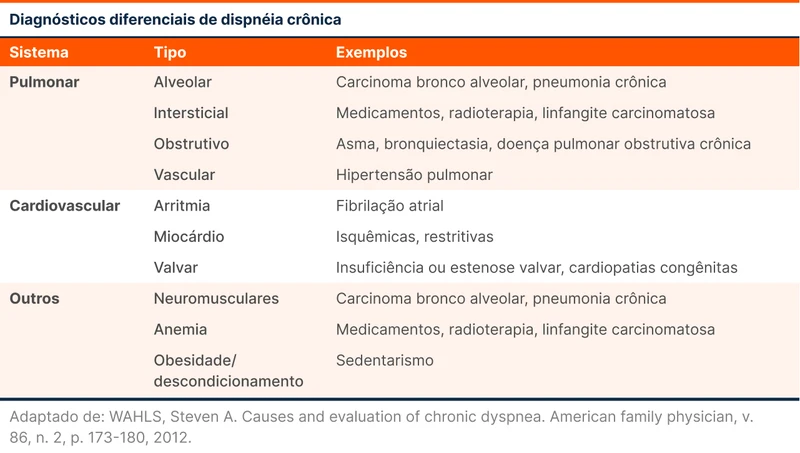
Dispneia é o sintoma principal do paciente e é uma queixa com muitos diagnósticos diferenciais. Pode ser secundária a alterações pulmonares, cardíacas, neuromusculares, anemia ou descondicionamento físico. Outros dados clínicos ajudam a estreitar as hipóteses. O primeiro deles é a temporalidade. Dispneia pode ser dividida em dois grupos: aguda, quando se inicia em horas a dias; e crônica, quando perdura por mais de quatro a oito semanas. O paciente tem dispneia crônica. A tabela 1 agrupa alguns diagnósticos diferenciais de dispneia crônica.
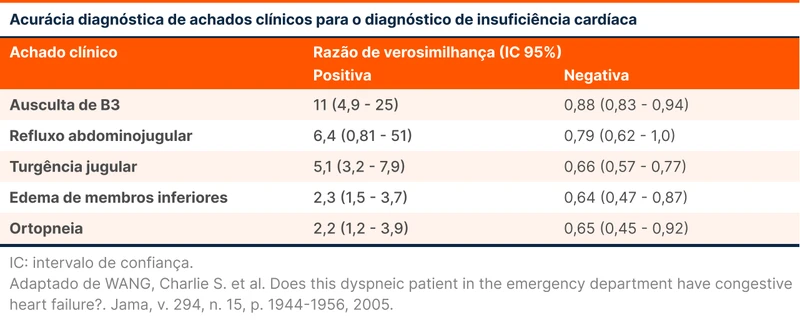
Outros dados clínicos sugerem que a dispneia tem origem cardíaca. Dentre eles, os que mais precisamente correlacionam os sintomas com causas cardíacas são a presença de B3 à ausculta e a presença do refluxo abdominojugular (ou hepatojugular). A tabela 2 traz achados clínicos e as razões de verossimilhança para o diagnóstico de insuficiência cardíaca.
O paciente também preenche os critérios de Framingham para o diagnóstico de insuficiência cardíaca (IC), abordados no caso clínico 7. Ascite e icterícia podem ser explicados por IC. Contudo, é prudente a avaliação de outras causas associadas, como hepatopatia.
Coronariopatia levando a cardiomiopatia isquêmica é a principal causa de IC no mundo, seguida por cardiomiopatia hipertensiva [1]. Em pacientes jovens sem comorbidades, outras causas de IC merecem consideração, como valvopatias e miocardites. Exames laboratoriais e ecocardiograma são necessários para avaliar essas possibilidades.
Apesar de IC ser uma explicação provável e comum, ela não explica todo o quadro. A perda de peso é um achado possível na IC, mas a presença de palidez e sudorese noturna, especialmente em um jovem previamente hígido, devem levar à consideração de outros diagnósticos diferenciais. É possível que a causa dos sintomas sistêmicos e da IC tenham alguma relação, já que a IC ainda não tem uma boa explicação nesse momento.
O paciente foi admitido no serviço para a realização de exames laboratoriais. Os resultados foram liberados enquanto o paciente aguardava a realização de exames de imagem.
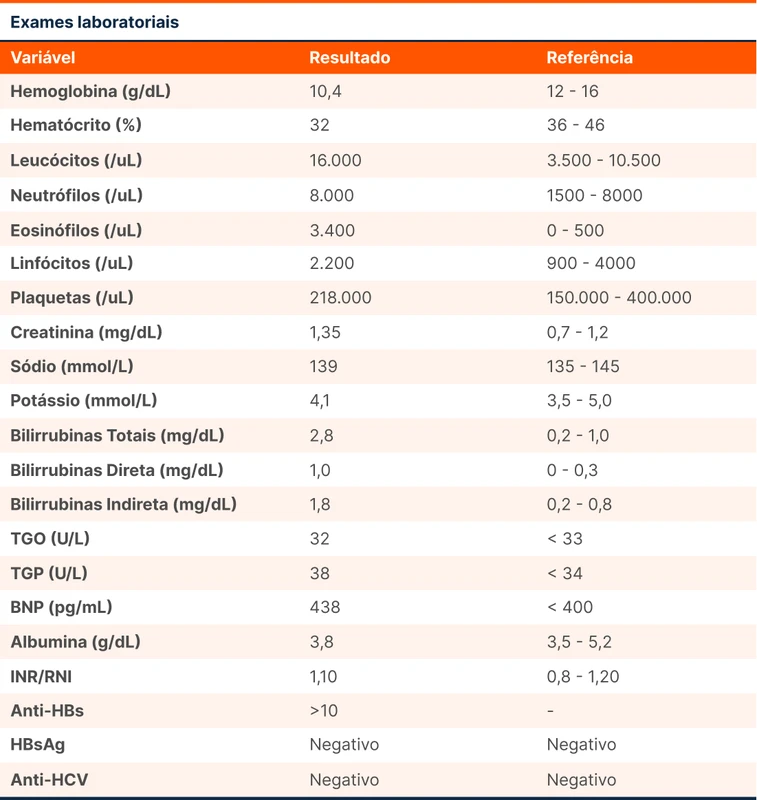
Os exames laboratoriais reforçam as hipóteses iniciais, mas levantam novas suspeitas. Como esperado, o paciente possui marcadores laboratoriais que sugerem insuficiência cardíaca, como o BNP. A icterícia pode ser secundária a uma hepatite congestiva. Na hepatite congestiva espera-se um aumento discreto de transaminases e um leve predomínio de bilirrubina indireta, com valores que não ultrapassam 3 mg/dL [2].
A eosinofilia não era um achado esperado. Muitas vezes os exames laboratoriais vêm com discretas alterações que nem sempre merecem investigação, podendo distrair do que realmente importa. Porém, um nível tão elevado de eosinófilos merece atenção. A contagem de eosinófilos considerada normal varia entre 50 a 500 células/μL, com valores maiores em neonatos e menores em adultos mais velhos [3]. A intensidade da eosinofilia é classificada como:
- Leve: limite superior da normalidade do laboratório até 1500 células/μL
- Moderada: 1500 a 5000 células/μL
- Grave: mais que 5000 células/μL
Além disso, quadros de eosinofilia podem ainda ser subclassificados em dois grupos [4]:
- Hipereosinofilia: presença de ≥ 1500 células/μL de forma persistente (dosados em duas ocasiões com intervalo de um mês)
- Síndrome hipereosinofílica: presença de ≥ 1500 células/μL de forma persistente associada a disfunções orgânicas atribuídas à eosinofilia. Casos com disfunções ameaçadoras à vida podem ser diagnosticados sem esperar um mês obrigatoriamente.
Além dos sintomas das doenças que causam eosinofilia, a própria eosinofilia pode lesionar sistemas orgânicos levando a alterações clínicas próprias. É exatamente esse processo que ocorre nas síndromes hipereosinofílicas, em que a infiltração tecidual de eosinófilos causa danos em diversos sistemas corporais. Os sistemas mais comumente acometidos pela síndrome hipereosinofílica são [5]:
- Dermatológico: manifestação comum ocorrendo na forma de eczema, eritrodermia, liquenificação e urticária.
- Pulmonar: pode ocorrer sibilância, mas também infiltrados pulmonares, derrame pleural e embolia pulmonar.
- Gastrointestinal: acometimento de qualquer parte do tubo digestivo levando a perda de peso, diarreia, dor abdominal, náuseas e hepatite.
- Cardíaco: importante causa de mortalidade, levando a miocardite eosinofílica.
- Neurológico: na forma de tromboembolismo, encefalopatia e neuropatia periférica.
Em todo paciente com eosinófilos maiores que 1500 células/μL deve-se procurar lesões de órgão-alvo comuns na síndrome hipereosinofílica. Na tabela 4 estão os principais exemplos de alterações clínicas que sugerem lesões sistêmicas. Em pacientes com sinais clínicos que possam ser atribuídos à eosinofilia, a avaliação complementar deve ser considerada mesmo se os valores forem menores que 1500 células/μL.

Em relação ao mecanismo, as eosinofilias podem ser primárias ou secundárias. As eosinofilias secundárias são as mais comuns e ocorrem de maneira reativa, quando os eosinófilos aumentam em resposta a algum estímulo. A eosinofilia primária é consequência de algum defeito na regulação da produção de eosinófilos levando à hiperproliferação dessa linhagem.
A anamnese deve procurar possíveis exposições a medicamentos, viagens, atividades recreacionais, dieta e condições de saneamento para direcionar a pesquisa de causas.
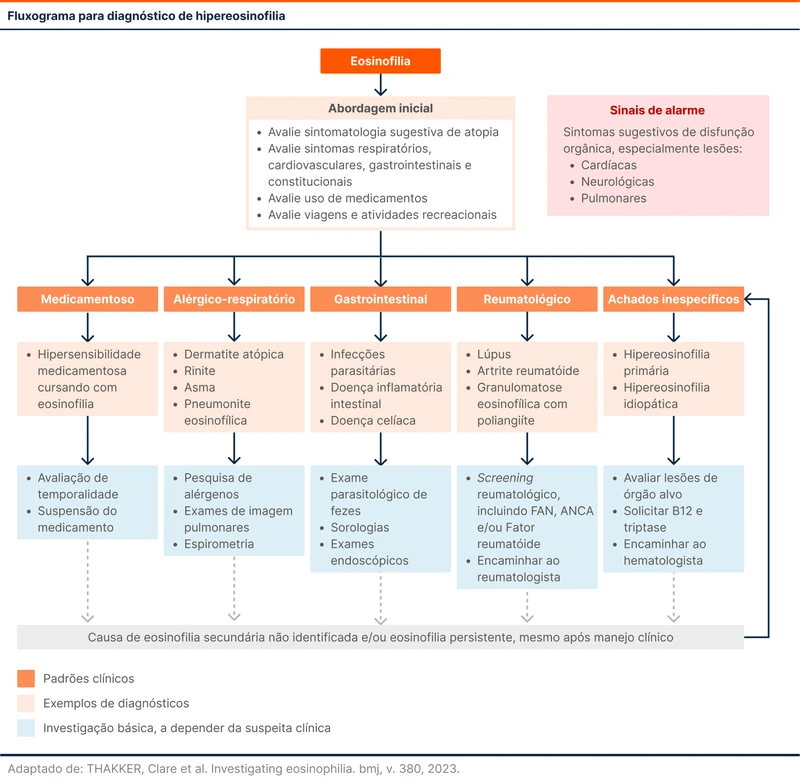
A eosinofilia pode aparecer combinada com outros achados clínicos. O fluxograma 1 exibe padrões, possíveis hipóteses e investigação complementar inicial para pacientes com eosinofilia.
Os achados do paciente mostram uma insuficiência cardíaca, o que é um sinal de alarme para a possibilidade de dano miocárdico consequente à eosinofilia. A miocardite eosinofílica é uma das principais causas de morbidade e mortalidade nos pacientes com síndrome hipereosinofílica, independente da etiologia. O ecocardiograma e os marcadores de lesão miocárdica devem ser realizados com urgência. Ainda na investigação da combinação de dispneia e eosinofilia, uma tomografia de tórax está indicada.
Foi realizada uma radiografia de tórax, que evidenciou sinais de congestão e leve aumento da área cardíaca, sem descrição de focos de consolidação. No ecocardiograma há descrição de fração de ejeção de ventrículo esquerdo de 69%, átrios de tamanho aumentado, disfunção diastólica de grau importante, falha de coaptação tricúspide, insuficiência mitral moderada e obliteração apical de ambos os ventrículos por massa hipoecogênica, podendo corresponder a fibrose ou formação trombótica. Tais achados são sugestivos de endomiocardiofibrose.
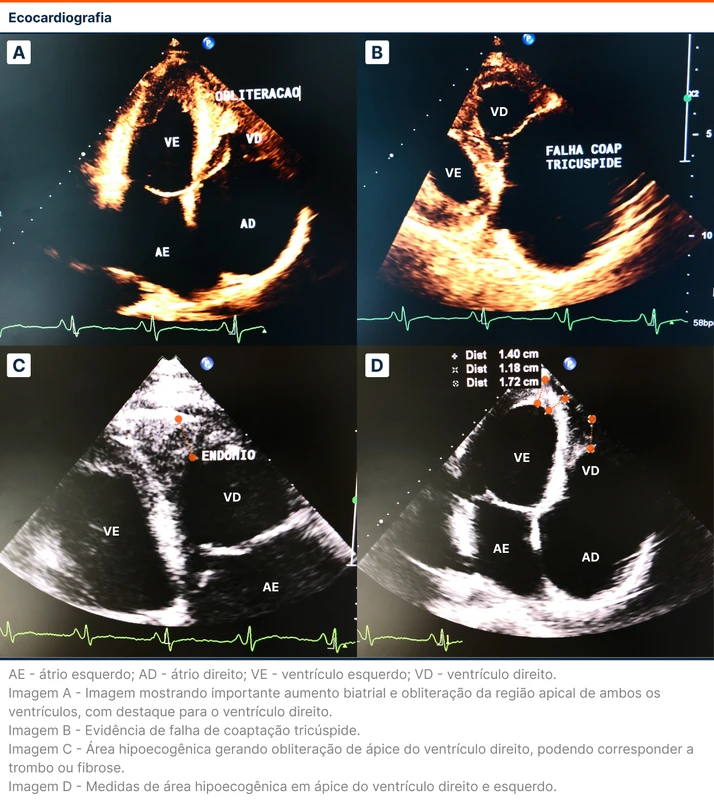
A ecocardiografia traz pistas diagnósticas. A combinação de achados de preservação de função sistólica, disfunção diastólica de padrão restritivo, obliteração ventricular bilateral por material hipoecogênico, que pode corresponder a fibrose ou formação trombótica, associado à comprometimento valvar mitral são padrões tipicamente descritos na endomiocardiofibrose. Esse tipo de cardiomiopatia faz parte do grupo das cardiomiopatias restritivas e possui algumas etiologias, dentre elas a síndrome hipereosinofílica. Além de disfunção miocárdica, a lesão por eosinófilos pode causar trombos e consequentes embolizações.
Com esses achados, fica indicado o tratamento de emergência para a síndrome hipereosinofílica. A terapia é com corticoides, variando a dose de 1 mg/kg de prednisona até 1 g de metilprednisolona, com base na intensidade dos achados clínicos. Deve-se considerar o tratamento empírico para estrongiloidíase, pois essa verminose pode fazer eosinofilia e ser agravada pela corticoterapia.
A tabela 5 mostra as indicações gerais de tratamento de emergência com corticoterapia na síndrome hipereosinofílica.

A etiologia do quadro ainda é desconhecida. Além da pesquisa de causas secundárias, é necessária a avaliação de possível neoplasia hematológica primária. Nessa pesquisa recomenda-se a dosagem de vitamina B12 e triptase - comumente elevadas nas variantes mieloproliferativas da síndrome hipereosinofílica - e pesquisa de mutações específicas na medula óssea e/ou em sangue periférico.
O paciente apresentou valores elevados de triptase e vitamina B12, reforçando a hipótese de variante mieloproliferativa para a síndrome hipereosinofílica. Após envio de material para estudo genético, foi evidenciada a fusão FIP1L1-PDGFRA, confirmando o diagnóstico de leucemia eosinofílica crônica [6]. Foi iniciado tratamento com imatinibe, com resposta sustentada da eosinofilia.
Alguns pontos de aprendizagem sobre o caso que você não pode esquecer:
- As eosinofilias devem ser investigadas com foco inicial em causas secundárias, incluindo avaliação de histórico de alergias, uso de medicações, hábitos de vida e presença de queixas respiratórias, gastrointestinais ou neurológicas.
- A presença de eosinofilia com valores elevados deve desencadear a pesquisa ativa de lesão de órgão alvo.
- O tratamento de urgência com corticoterapia deve ser considerado em pacientes com eosinofilia e sinais de dano orgânico, especialmente cardíaco, pulmonar ou neurológico.
- A endomiocardiofibriose é uma cardiomiopatia restritiva que possui forte associação com a eosinofilia. É definida pelo padrão restritivo, trombose e/ou fibrose em região apical dos ventrículos, alargamento atrial e insuficiência mitral e/ou tricúspide secundárias a um tracionamento dos folhetos valvares.
- A investigação inicial das eosinofilias primárias inclui a solicitação de triptase e vitamina B12 e avaliação hematológica especializada. Dentre os achados, a presença da fusão FIP1L1-PDGFRA confirma o diagnóstico de leucemia eosinofílica crônica.
Aproveite e leia:
Gamopatia Monoclonal de Significado Indeterminado (MGUS)
A gamopatia monoclonal de significado indeterminado (MGUS) é uma condição pré-maligna com risco de evoluir para neoplasia hematológica, principalmente mieloma múltiplo. A maioria dos pacientes com MGUS não progredirá para quadros neoplásicos, dificultando a escolha de quem se beneficiaria de investigação adicional. Em abril de 2024, foi publicado no Annals of Internal Medicine uma calculadora de risco para auxiliar na indicação de investigação medular nesses pacientes. Este tópico revisa MGUS e traz os resultados do estudo.
Trombocitopenia Induzida por Heparina
A trombocitopenia induzida por heparina é potencialmente fatal e envolve redução de plaquetas com eventos trombóticos. Em março de 2024, o JAMA Open publicou um artigo que avaliou a acurácia da abordagem diagnóstica dessa condição. Este tópico revisa a definição, apresentação clínica e abordagem terapêutica da trombocitopenia induzida por heparina.
Caso Clínico #7
Um homem de 65 anos com dispneia e cardiomegalia, evolui com hemorragia digestiva e hematomas.
Linfoma de Burkitt
O linfoma de Burkitt é um linfoma agressivo com manifestações clínicas expressivas. Aproveitando uma revisão recente do New England Journal of Medicine, vamos passar pelos principais pontos dessa doença.
Manejo de Sangramento Maior em Pacientes em Uso de Anticoagulante Oral
Sangramento é o principal evento adverso dos anticoagulantes e deve ser rapidamente identificado e manejado. Em julho de 2023, foi lançado um consenso no European Journal of Emergency Medicine sobre o tratamento de sangramento maior em pacientes em uso de anticoagulantes orais. Este tópico revisa a definição de sangramento maior e as estratégias para reverter a anticoagulação.
