Asma - GINA 2023
Este tópico foi atualizado. Acesse "Atualização de Asma: GINA 2024" para ver as novidades.
Definição e padrões
A asma possui três características fundamentais:
- Presença de sintomas respiratórios como sibilos, tosse, dispneia e opressão torácica
- Variação de intensidade dos sintomas ao longo de um período
- Limitação no fluxo aéreo de forma reversível, que pode ser documentada de diversas formas
Essa definição é baseada na apresentação da doença antes do início da terapia com corticoide inalatório. Pacientes que já estão em tratamento podem não apresentar a reversão na limitação ao fluxo aéreo e ter sintomas mais brandos.
Existem alguns padrões de asma que se associam a grupos demográficos, comportamento clínico e fisiopatologia distintas. Esses padrões são também chamados de fenótipos e os mais comuns são:
- Asma alérgica: forma mais comum da doença, iniciada na infância e associada a dermatite atópica, rinite alérgica e alergia alimentar. Geralmente tem IgE total sérica elevada e IgE específica para aeroalérgenos ou prick test positivo. Junto com a asma eosinofílica compõem o grupo da inflamação do tipo T2 alto.
- Asma não alérgica: asma sem associação com outras doenças alérgicas. O escarro pode conter menos células inflamatórias (paucigranulocítica) ou ter um perfil neutrofílico. Comumente são mais resistentes ao corticoide inalatório.
- Asma de início na vida adulta: Alguns adultos tendem a se apresentar com asma de início mais tardio. Costumam precisar de maiores doses de corticoide inalatório para controle da doença. Asma ocupacional e asma associada a medicamentos devem ser procuradas. Até 16% desses pacientes apresentam remissão total da doença em cinco anos.
- Asma com limitação persistente do fluxo aéreo: pacientes com asma não controlada por longos períodos podem não apresentar a reversibilidade na limitação do fluxo aéreo devido ao remodelamento das vias aéreas.
- Asma relacionada à obesidade: geralmente com sintomas respiratórios exuberantes, associada a inflamação não eosinofílica. Maior resistência ao uso de corticoide inalatório.
Diagnóstico
Idealmente todo paciente deve ser diagnosticado antes do início da terapia com corticóide inalatório. A medicação pode reduzir ou mascarar os sintomas respiratórios e normalizar a prova broncodilatadora.
Familiares com asma e a presença de outras doenças atópicas favorecem o diagnóstico. Alguns sintomas são mais específicos de asma, como sibilos, dispneia, tosse e opressão torácica, especialmente quando têm as seguintes características:
- Mais de um desses sintomas em associação;
- Sintomas piores à noite ou no início da manhã, o que significa variação no tempo e em intensidade;
- Os sintomas são desencadeados ou exacerbados por infecções virais, exposição a aeroalérgenos, mudança de temperatura, tabagismo ou outras exposições.
Algumas características devem levantar a suspeita de diagnósticos diferenciais. As principais são as seguintes:
- Tosse como um sintoma isolado
- Expectoração abundante
- Dispneia associada a lipotimia, cefaleia ou parestesias
- Dor torácica
- Dispneia induzida por exercícios associada a estridor
Quando esses sintomas estão presentes, sugerem outras patologias, conforme evidenciado na tabela 1.
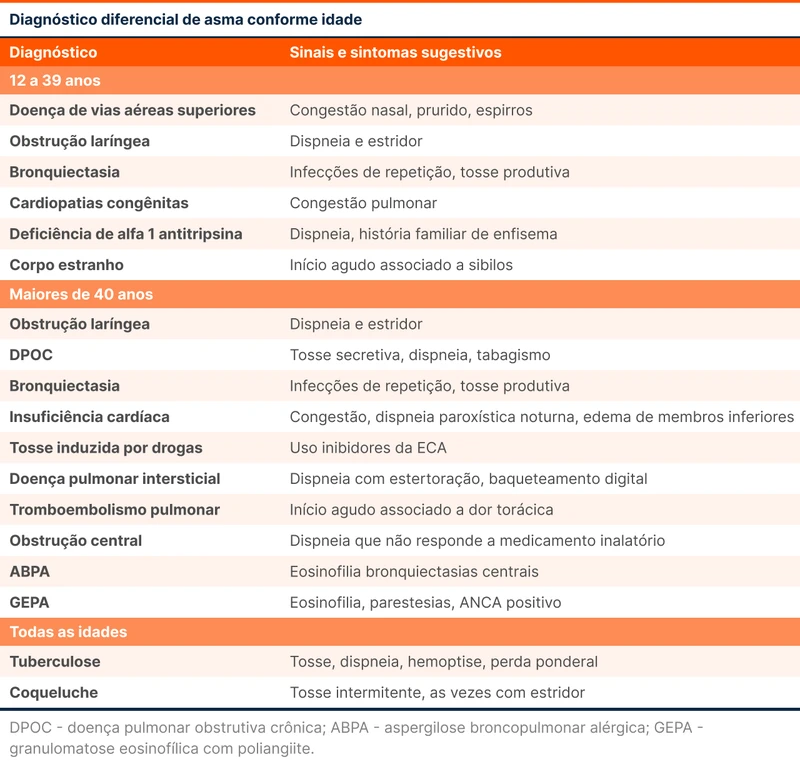
Asma de início da idade adulta deve levantar duas suspeitas: asma ocupacional e doença pulmonar obstrutiva crônica (DPOC). Asma ocupacional pode representar até 20% das causas de asma em adultos. O principal tratamento é afastar o paciente da atividade envolvida na exposição. Pode ser difícil diferenciar asma de DPOC, especialmente em tabagistas. Variação na intensidade dos sintomas, prova broncodilatadora fortemente positiva e capacidade de difusão do monóxido de carbono aumentada ou "normal-alta" sugerem asma [3].
A confirmação diagnóstica com espirometria é importante para evitar diagnósticos e tratamento em excesso e identificar diagnósticos diferenciais.
Espirometria
Espirometria com prova broncodilatadora é o exame mais utilizado para documentar a limitação variável do fluxo aéreo. Considera-se uma prova broncodilatadora positiva quando o volume expiratório forçado no primeiro segundo (VEF1) aumenta em 200 ml E 12% do valor pré broncodilatador. Esse não é o único critério entre as diretrizes. A European Respiratory Society e a American Thoracic Society (ERS/ATS) sugerem utilizar o aumento de 10% do previsto no VEF1 como critério para definir uma prova broncodilatadora positiva [4].
Pacientes que já estão em uso de corticoide inalatório podem apresentar prova broncodilatadora negativa. Nessa situação, duas estratégias podem ser usadas para revelar o diagnóstico de asma. Na primeira, comparam-se espirometrias pré e pós início do corticoide inalatório, quando disponíveis. Pacientes com acréscimo no VEF1 de 200ml E 12% do valor pré broncodilatador quatro semanas após a medicação, podem ser considerados como tendo prova broncodilatadora positiva.
A segunda opção sugerida pelo GINA é a realização do step down - que consiste na redução ou suspensão momentânea do corticoide inalatório para realização da espirometria. Para isso, o paciente deve ter bom controle da asma e não possuir fatores de risco para exacerbações. Geralmente é realizada redução da dose de corticoide inalatório entre 25 a 50% ao longo de 3 meses.
Além dos valores de VEF1 na espirometria, outras avaliações sugerem o diagnóstico de asma:
- Variação do peak flow diurno maior que 10%;
- Melhora da função pulmonar em 200 ml E 12% do valor pré broncodilatador em adultos submetidos a espirometria após 4 semanas de tratamento;
- Variação no VEF1 em 20% durante o teste de broncoprovocação com metacolina ou 15% com hiperventilação, manitol ou salina hipertônica;
- Variação na espirometria entre consultas;
- Teste do exercício positivo, com queda de 10% no VEF1 E 200 ml após exercício.
Após documentar a variabilidade é importante verificar se a relação do VEF1/CVF também se encontra reduzida, caracterizando obstrução. O GINA sugere utilizar o limite inferior da normalidade. Em adultos, esse valor geralmente corresponde a uma relação entre 0.75 e 0.80. A espirometria com obstrução sem prova broncodilatadora positiva não exclui asma.
Asma no ambulatório: avaliação
A avaliação do controle da asma é feita por dois principais critérios: controle de sintomas e o risco de exacerbações.
O controle de sintomas pode ser avaliado com questionários como o Asthma Control Test (ACT), ou perguntando sobre sintomas nas quatro semanas anteriores à consulta. Ao questionar o paciente sobre sintomas, quatro variáveis são definidoras:
- Presença de despertar noturno
- Presença de sintomas diurnos mais de duas vezes na semana
- Uso de medicação de resgate mais do que duas vezes na semana
- Limitação nas atividades diárias
Com essas informações é possível classificar o controle da asma do paciente:
- Asma controlada: ausência dos sintomas interrogados nas últimas quatro semanas
- Asma parcialmente controlada: presença de um ou dois dos sintomas interrogados nas últimas quatro semanas
- Asma não controlada: presença de três ou quatro dos sintomas interrogados nas últimas quatro semanas.
O risco de exacerbações deve ser avaliado procurando ativamente fatores de risco. O maior fator de risco é o controle inadequado dos sintomas. Outros fatores são: uso frequente de SABA (beta agonista de curta ação) de resgate, má adesão ou prescrição inadequada de corticoide inalatório, VEF1 inferior a 60%, tabagismo, obesidade, fração exalada de óxido nítrico (FeNO) elevada, eosinofilia, exacerbação grave com necessidade de intubação no último ano. A tabela 2 agrupa estes e outros critérios de risco para exacerbações.

A avaliação do controle de sintomas e do risco de exacerbações deve ser registrada separadamente em prontuário. Um paciente pode ter ao mesmo tempo bom controle de sintomas e alto risco de exacerbações, precisando de maior vigilância.
O acompanhamento do paciente com asma também deve ser realizado com a espirometria. Recomenda-se, além do exame feito ao diagnóstico, sua repetição três a seis meses após atingir dose estável de corticoide inalatório. Posteriormente, a cada um ou dois anos.
A asma deve ser classificada quanto a gravidade. A gravidade ajuda a identificar quais pacientes se beneficiam de terapia adicional, como imunobiológicos. Essa classificação é retrospectiva e depende de qual tratamento foi necessário para controlar a doença:
- Asma leve: controlada com baixa dose de corticoide inalatório ou corticoide-formoterol quando necessário - steps 1 e 2 do GINA. O termo "asma leve" vem sendo desencorajado, pois pode reduzir a adesão ao tratamento por fazer o paciente minimizar sua condição. O maior problema desse termo é que a asma leve pode levar a exacerbações graves.
- Asma moderada: controlada em uso de corticoide inalatório-LABA (beta agonista de longa ação) em dose baixa ou moderada - steps 3 e 4 do GINA.
- Asma grave: asma não controlada com dose elevada de corticoide-LABA ou controlada apenas com altas doses de corticoide-LABA. Quando o paciente precisa dessas doses, inicialmente é classificado como asma de difícil controle. Nessa situação, sempre devem ser avaliadas comorbidades, dificuldade de adesão e tratamento inadequado dos sintomas. Após a exclusão desses fatores, a asma de difícil controle é caracterizada como asma grave. Cerca de 3,7% dos pacientes entram nesse grupo de acordo com o GINA. Todo paciente com asma grave deve ser referenciado ao especialista para fenotipagem e seguimento.
O objetivo do tratamento é atingir bom controle de sintomas, reduzir o risco de exacerbações, mortalidade e obstrução persistente do fluxo aéreo. A principal medicação é o corticoide inalatório (ICS). O uso de broncodilatadores de forma isolada, principalmente de curta duração, se correlaciona com maior risco de exacerbações (veja o tópico sobre Asma e Uso de Beta Agonistas de Curta Ação).
A terapia inalatória deve ser ajustada periodicamente, em geral a cada três meses. A depender do controle, o paciente pode subir ou descer nos steps do tratamento.
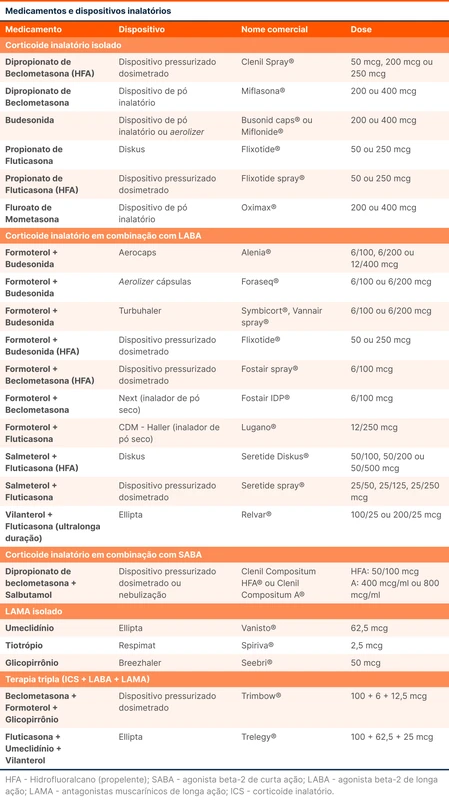
A tabela 3 apresenta as formulações, doses e dispositivos dos principais corticoides inalatórios, corticoides em combinação com LABA, corticoides em combinação com SABA, corticoides em associação com LAMA (antimuscarínico de longa ação) e LAMA isoladamente.
Steps 1 e 2
O GINA propõe duas "vias" ou "tracks" possíveis - a via preferencial deve ser utilizada quando as formulações com formoterol estão disponíveis. A principal diferença do formoterol para os outros LABAs é que ele possui um rápido início de ação, apesar de ser um beta agonista de longa duração. Isso permite que ele seja usado para manutenção e para alívio, dispensando a necessidade de SABA para alívio.
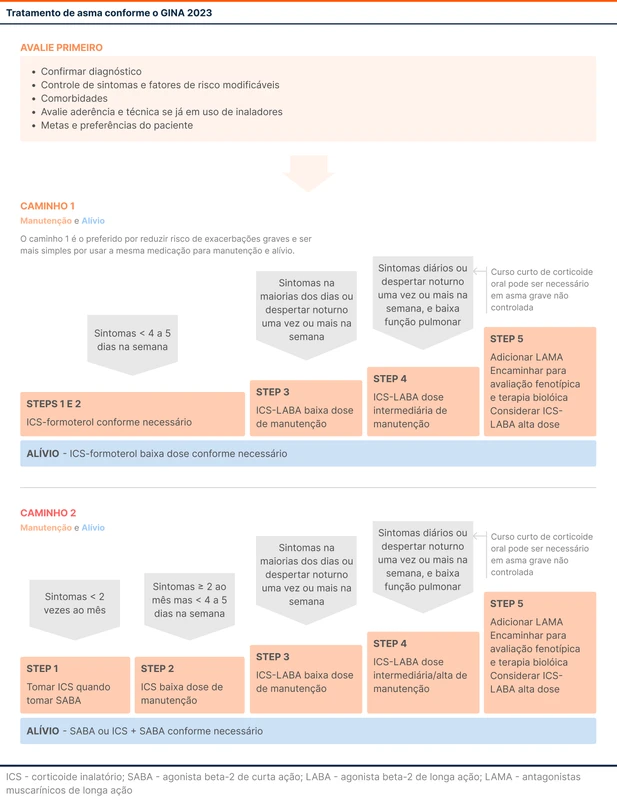
Step 1
O step 1 deve ser escolhido quando o paciente apresenta sintomas menos de duas vezes ao mês. Pode-se utilizar ICS-formoterol em baixa dose quando necessário ou fazer uso de ICS associado a SABA caso a opção seja pela via alternativa. O GINA 2023 também deixa como opção o uso de ICS-SABA como medicação de resgate, uma novidade em relação à edição de 2022 em que as medicações eram oferecidas em dispositivos separados.
Step 2
Indicado quando o paciente apresenta mais de dois episódios sintomáticos ao mês, porém menos de quatro a cinco vezes por semana. Na via preferencial com formoterol, os steps 1 e 2 são iguais. Ambos utilizarão ICS-formoterol sempre que precisarem para alívio. Essa estratégia traz a vantagem de controle de sintomas com o formoterol e redução de exacerbações por causa da maior dose de corticoide inalatório.
Na via alternativa, o indicado é utilizar um corticoide inalatório de manutenção associado a SABA ou SABA+ICS sempre que necessário. O uso de corticoide de manutenção diário está associado a maior controle de sintomas do que o ICS-formoterol apenas quando necessário, porém como se trata de uma medicação de uso diário, a adesão é menor [5].
Steps 3 e 4
Step 3
É a escolha quando o paciente possui sintomas na maioria dos dias ou quando é acordado por sintomas da doença pelo menos uma vez por semana. Nesse caso, na via preferencial, utiliza-se uma estratégia conhecida como MART (maintenance-and-reliever therapy). Na MART o tratamento de manutenção e o de alívio são realizados com ICS-formoterol em dose baixa.
A via alternativa é escolhida quando não há formoterol, utilizando-se um ICS-LABA em dose baixa como manutenção. A terapia de alívio é feita com SABA ou SABA+ICS, uma vez que os demais beta agonistas de longa duração não apresentam um efeito tão imediato para alívio quanto o formoterol.
Step 4
Inclui pacientes que apresentam sintomas na maioria dos dias ou são acordados por sintomas da doença pelo menos uma vez na semana, além de possuírem comprometimento de função pulmonar.
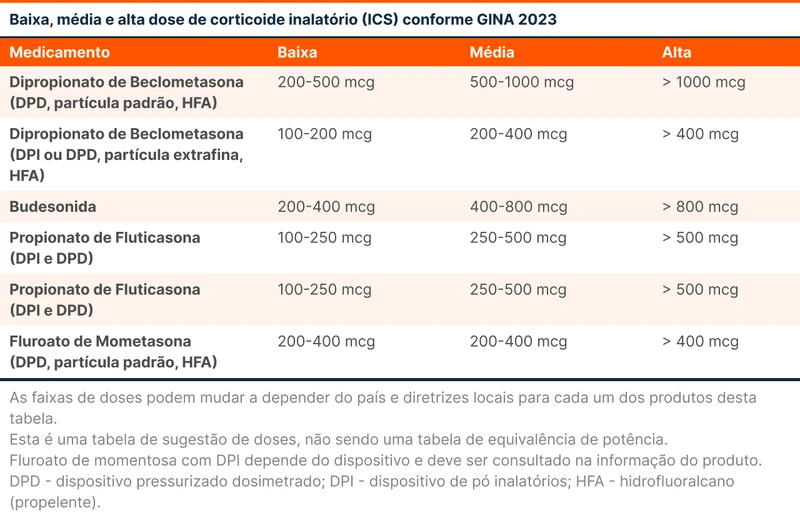
No caso da via preferencial, utiliza-se ICS-formoterol em dose moderada e como alívio, enquanto na via alternativa a orientação é de um ICS-LABA em dose moderada a alta e SABA ou SABA+ICS como alívio. A tabela 4 disponibiliza as doses de cada um dos corticoides inalatórios e a dosagem que os classifica em baixa, moderada ou alta dose.
Step 5
Caso o paciente chegue ao step 4 e ainda esteja com asma não controlada ou parcialmente controlada, deve-se progredir o tratamento para o step 5. Nesse momento o GINA orienta o início de um LAMA. Estudos indicam que o LAMA nessa população melhora discretamente a função pulmonar e o risco de exacerbações, porém sem melhora significativa nos sintomas ou na qualidade de vida [6].
Todo paciente que esteja no step 5 deve ser referenciado para o especialista para fenotipagem, geralmente utilizando dosagem de IgE total, prick test ou IgE específico para aeroalérgenos, eosinófilos séricos e do escarro e fração de óxido nítrico exalada (FeNO). Após essa avaliação, três fenótipos são descritos:
- Asma grave alérgica: IgE total elevada, prick test ou IgE específica positivos.
- Asma eosinofílica: eosinófilos séricos acima de 150, eosinofilia do escarro maior que 2-3%, FeNO acima de 20 ppm.
- Asma não eosinofílica: eosinófilos séricos ou no escarro baixos, IgE baixa.
Fenotipar o paciente indica a via de inflamação predominante para auxiliar na escolha do imunobiológico, quando indicados. Atualmente estão disponíveis as seguintes opções:
- Anti-IgE: omalizumabe, utilizado para as formas predominantemente alérgicas
- Anti-IL5: mepolizumabe, reslizumabe e benralizumabe são escolhas para o subtipo eosinofílico
- Anti-IL4/13: dupilumabe, também pode ser utilizado na asma eosinofílica, especialmente quando o FeNO for elevado ou estiver associado a dermatite atópica e/ou esofagite eosinofílica.
- Anti-TSLP: tezepelumabe. Atua no início da cascata de inflamação em uma citocina presente no epitélio e portanto pode ser utilizada para qualquer subtipo de asma, inclusive a neutrofílica/paucigranulocítica.
Apenas uma minoria dos pacientes apresentam realmente asma grave. Antes de considerar terapias avançadas, sempre devem ser investigadas comorbidades (doença do refluxo, tabagismo, apneia do sono, polipose nasal, etc), garantir a técnica inalatória e adequação do dispositivo para o paciente.
Asma exacerbada: avaliação
Exacerbação é a piora aguda ou subaguda dos sintomas e da função pulmonar em relação ao basal. Muitas vezes o diagnóstico de asma é suspeitado durante uma exacerbação.
O fator desencadeante da exacerbação deve ser procurado. Alguns exemplos de desencadeantes são:
- Infecções virais ou bacterianas
- Exposição a alérgenos como poeira, mofo e outros
- Alergia alimentar
- Dificuldades de adesão
- Mudanças sazonais
- Poluição ambiental
Os sintomas mais comuns são piora da dispneia associada a sibilos e tosse. Muitos pacientes com asma também possuem alergia alimentar, e os sintomas de asma exacerbada podem ser confundidos com anafilaxia. A distinção entre as condições não é simples e a administração de adrenalina não deve ser atrasada em caso de dúvida.
Algumas pessoas, especialmente homens e pacientes com asma grave não controlada, podem não perceber o agravamento dos sintomas. Esses pacientes tendem a chegar no pronto socorro com sintomas mais graves.
A forma mais objetiva de documentar a piora da função pulmonar é através da medida do pico de fluxo expiratório (peak flow), que pode ser realizado a partir dos cinco anos de idade. Um resultado inferior a 50% do predito classifica a exacerbação como grave. A aferição do pico de fluxo também auxilia a avaliar a resposta ao tratamento e pode ser repetida quantas vezes forem necessárias durante o atendimento.
A gasometria arterial é reservada para casos selecionados. Pacientes com pico de fluxo expiratório inferior a 25% do predito ou em insuficiência respiratória devem ter gasometria arterial coletada. O exame confirma a saturação de oxigênio e fornece a pCO2. Elevação da pCO2 indica hipoventilação e redução do volume-minuto, podendo significar fadiga respiratória.
A radiografia de tórax também não deve ser solicitada de rotina. Seu papel na asma exacerbada é para descartar diagnósticos diferenciais como insuficiência cardíaca descompensada, pneumotórax, pneumonia e atelectasias [7]. Deve ser considerada em pacientes que não estão respondendo à terapia.
A exacerbação da asma deve ser classificada de acordo com a gravidade. Essa classificação é feita com base em parâmetros clínicos, exclusivamente.
Nas exacerbações leves ou moderadas o paciente consegue falar frases completas, não se apresenta agitado, não utiliza musculatura acessória e possui frequência cardíaca entre 100 e 120 bpm.
Exacerbações graves são aquelas em que o paciente consegue falar apenas palavras, se mostra agitado durante a avaliação, possui frequência respiratória superior a 30 ipm ou frequência cardíaca maior que 120 bpm, utiliza musculatura acessória ou apresenta saturação em ar ambiente menor que 90%. Qualquer um desses já caracteriza a exacerbação como grave.
Asma exacerbada: tratamento
As medidas que trazem maior benefício no tratamento da exacerbação são o SABA e corticoide sistêmico.
Devem ser usados 4-10 puffs de SABA por inalador dosimetrado em conjunto com o espaçador, a cada 20 minutos na primeira hora. O uso do espaçador facilita a administração, já que pacientes em exacerbação podem não conseguir fazer uma inspiração forçada adequada para a técnica correta. A dose recomendada de prednisolona é de 40 a 50 mg por 5 a 7 dias e pode ser iniciada durante o atendimento na emergência.
Quatro parâmetros devem estar presentes para alta médica:
- Melhora sintomática, sem necessidade do uso de SABA para alívio
- Saturação em ar ambiente > 94%
- Melhora no pico de fluxo, idealmente acima de 60-80% do previsto (ou melhora em relação ao basal do paciente)
- Condições socioeconômicas para alta
Pacientes com exacerbação grave devem ser transferidos para unidades com possibilidade de monitorização e vigilância intensiva.
A primeira decisão em pacientes com exacerbação grave é quanto à necessidade de intubação. O uso de ventilação não invasiva não mostrou benefício claro na asma exacerbada, mas pode impedir uma intubação. A intubação não deve ser atrasada em casos de indicação evidente, especialmente em pacientes com redução importante do nível de consciência.
Na exacerbação grave também são usados SABA e corticoides sistêmicos. A depender das condições clínicas do paciente, a via intravenosa pode ser preferida.
Na exacerbação grave existe benefício do uso de SAMA. Estudos demonstraram aumento do pico de fluxo expiratório e redução de hospitalizações quando associados ao SABA [8].
O sulfato de magnésio intravenoso pode ser usado em exacerbações graves, com VEF1 menor que 25 a 30% e que mantêm hipoxemia após as medidas iniciais. Deve ser administrado em dose única de 2 gramas em 20 minutos [9].
Pacientes que mantêm pico de fluxo expiratório inferior a 60% do previsto e sem melhora dos sintomas devem ser internados. Em pacientes com pico de fluxo expiratório superior a 60 a 80% do previsto e melhora sintomática é possível considerar alta hospitalar com reavaliação precoce.
Todos os pacientes devem ser submetidos a reavaliação do tratamento após uma exacerbação. Nessa ocasião pode ser considerado aumento da medicação de manutenção por pelo menos uma a duas semanas após o evento.
Aproveite e leia:
Atualização de Asma: GINA 2024
Anualmente é publicada a diretriz do Global Initiative for Asthma (GINA), um programa internacional sobre prevenção, diagnóstico e tratamento do paciente com asma. Este tópico traz as atualizações do GINA 2024.
Novos Critérios Diagnósticos e Classificação da Obesidade
Uma nova proposta de critérios para o diagnóstico e classificação da obesidade foi publicada no Lancet em janeiro de 2025. Este tópico aborda essa nova publicação.
Avaliação de Dor Torácica Estável com Angiotomografia
Em abril de 2022, o New England Journal of Medicine publicou o trabalho DISCHARGE comparando o uso de angiotomografia de coronárias com cineangiocoronariografia para avaliação de dor torácica estável. Vamos ver o que essa nova evidência acrescenta.
Nova Definição de Síndrome do Desconforto Respiratório Agudo (SDRA)
A síndrome do desconforto respiratório agudo (SDRA) é uma das principais causas de internação em UTI. Em julho de 2023 foi proposta uma nova definição global sobre SDRA. Esse tópico explica as mudanças, comentando as vantagens e desvantagens da nova definição.
Doença de Graves: Mudanças no Diagnóstico e Tratamento
A doença de Graves é a causa de até 70% dos casos de hipertireoidismo, com incidência anual de 30 a 50 casos por 100.000 habitantes. Um artigo da Endocrine Society publicado em 2024 observou mudanças no diagnóstico e tratamento da doença na última década. Este tópico revisa o diagnóstico, sintomas mais comuns e modalidades de tratamento utilizadas atualmente.
