Neoplasia de Testículos
A neoplasia de testículo é uma das neoplasias mais comuns da população jovem. Em novembro de 2022 o British Medical Journal publicou uma revisão sobre os avanços da abordagem dessa doença [1]. Nesse "Síndromes e Cenários", trazemos os principais pontos discutidos na publicação.
Epidemiologia e fatores de risco de neoplasia de testículo
Tumor de testículo é a neoplasia mais comum do paciente jovem, com incidência crescente nos últimos anos. O Instituto Nacional do Câncer (INCA) informa que a neoplasia de testículo corresponde a 5% de todas as neoplasias na faixa etária de 15 a 29 anos [2]. Em contrapartida, tem boas taxas de resposta a terapia, atingindo 95% de cura em todos os pacientes e 80 a 90% de cura em pacientes com metástase.
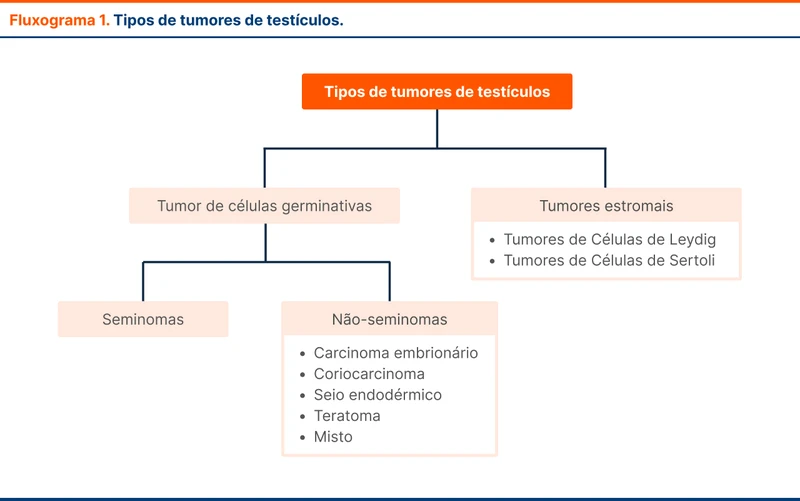
Dentre os tipos de tumores de testículo, o mais comum é tumor de células germinativas, correspondendo a 95% dos casos. Os outros 5% são os tumores estromais, como o tumor de células de Leydig e o de células de Sertoli. Estes últimos são geralmente benignos.
Os tumores de células germinativas podem ser subdivididos em seminomas e não seminomas. Tumores não seminomas são, em geral, mais agressivos e são classificados em quatro tipos: carcinoma embrionário, coriocarcinoma, seio endodérmico e teratoma (ver fluxograma 1). A análise histopatológica pode mostrar células de seminomas e de não seminomas. Nesse caso, a neoplasia se comporta e é tratada como um não seminoma.
Dentre os fatores de risco, destaca-se o componente genético. Irmãos de pacientes com neoplasia de testículo têm 8 a 10 vezes maior risco de desenvolver a doença [3]. Outros fatores de risco incluem história de criptorquidia na infância e atraso na sua correção - especialmente após os 13 anos de idade.
Quais são os sintomas?
O sintoma local de maior destaque é a detecção de uma massa testicular. Também pode ocorrer dor lombar por infiltração de linfonodos retroperitoneais ou sintomas relacionados a metástases, como manifestações pulmonares e de sistema nervoso central.
Ginecomastia é um sintoma mais presente no tumor de células de Leydig, mas pode ocorrer nos tumores de células germinativas [4]. A neoplasia de testículo pode se manifestar com síndromes paraneoplásicas. Entre elas estão o hipertireoidismo paraneoplásico, em consequência da hiperprodução de gonadotrofina coriônica humana (hCG) que tem ação estimuladora da tireoide, e a encefalite límbica, secundária ao anticorpo anti-Ma2.
A infertilidade pode aparecer antes do surgimento de massa palpável. Uma série de 4418 casos de infertilidade encontrou 46 lesões testiculares assintomáticas e menores que 10 mm [5].
Quais são os exames complementares?
O ultrassom é o exame inicial de escolha. A neoplasia de testículo pode se apresentar como massa hipoecoica, com calcificação ou com margens irregulares. A presença de lesão sugestiva de neoplasia testicular é uma indicação de orquiectomia para fins diagnósticos e terapêuticos. A biópsia não deve ser realizada, pelo risco de contaminação por células neoplásicas no escroto e na drenagem linfática. Não é recomendada a biópsia de outro testículo em todos os pacientes, mas pode ser realizada em pacientes de alto risco, como aqueles com volume testicular menor que 12 ml e/ou história de criptorquidia.
A dosagem de β-hCG e alfa-fetoproteína (AFP) no momento do diagnóstico aumenta a suspeita de tumor de testículo, mas não deve ser usada como confirmação ou exclusão da doença. O β-hCG e a AFP se elevam nos tumores não seminomas. Nos seminomas, o β-hCG se eleva apenas em 20% dos pacientes e a AFP não se eleva. Seu papel é mais estabelecido na avaliação de controle de doenças após tratamento. A desidrogenase láctica é útil para avaliar a extensão da doença.
A investigação prossegue com exames de imagem de tórax, abdome e pelve para detecção de metástases. Uma metanálise apontou que 47% dos pacientes com invasão linfovascular no anatomopatológico tinham metástases ocultas [6].
Os principais locais de metástases são pulmões, ossos, fígado e sistema nervoso central [7]. As metástases para o sistema nervoso central são quase exclusivamente de tumores não seminomas. De todas as metástases cerebrais, 2 a 3% são devido à neoplasia testicular.
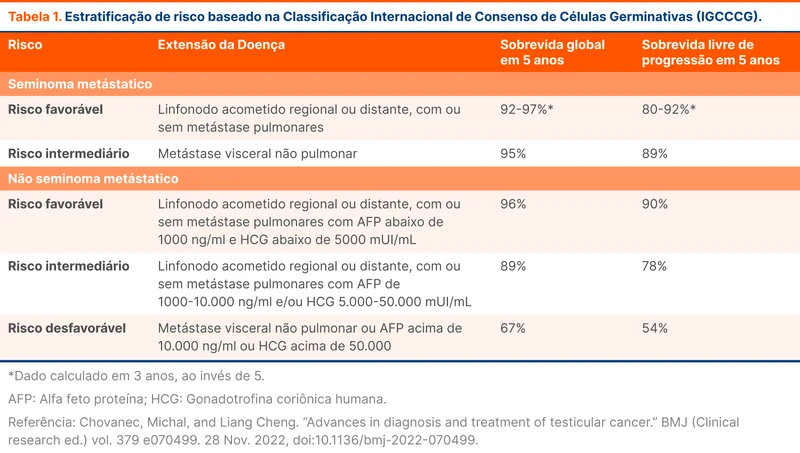
Ressonância magnética é o exame de escolha para detecção de metástase cerebral. Nesse cenário, deve ser utilizada se o paciente tem presença de sintomas ou se apresenta em uma categoria de risco desfavorável, avaliada pela escala do do International Germ Cell Cancer Collaborative Group (IGCCCG), visto na tabela 1.
Como é o tratamento?
O tratamento possui como base a orquiectomia, quimioterapia adjuvante e radioterapia.
A orquiectomia é utilizada com objetivo diagnóstico e terapêutico. Os níveis dos marcadores tumorais (β-hCG e AFP) após a orquiectomia irão compor o estadiamento do paciente (tabela 1). A maioria dos pacientes se apresenta como estágio 1 e a cirurgia pode ser suficiente para atingir cura.
Quimioterapia adjuvante pode ser realizada desde o estágio 1 a depender do subtipo do tumor e de marcadores prognósticos. Os esquemas principais envolvem carboplatina, ou uma combinação de cisplatina, bleomicina e etoposídeo. A bleomicina é contraindicada em pacientes com carga tabágica alta, disfunção renal ou idade acima de 50 anos. Nesses casos, é substituída por ifosfamida.
A radioterapia é utilizada para o tratamento de linfonodos retroperitoneais. Deve ser reservada para casos selecionados, pois a radioterapia aumenta em duas a seis vezes o risco do paciente apresentar uma segunda neoplasia nos próximos 10 a 16 anos. Outra opção para o tratamento de metástase linfonodal é a cirurgia para a ressecção de linfonodos retroperitoneais.
Aproveite e leia:
Psilocibina para Depressão Resistente
Depressão resistente é um desafio de tratamento. Muitas pesquisas têm estudado os alucinógenos nesse contexto. Um estudo de fase 2 publicado em novembro no New England Journal of Medicine (NEJM) testou várias doses de psilocibina, um alucinógeno presente em cogumelos, para depressão resistente. Vamos revisar esse tema e ver os resultados do trabalho.
Reposição de Testosterona e Risco Cardiovascular
O uso de testosterona tem controvérsias, entre elas a relação a complicações cardiovasculares. Em julho de 2023 o New England Journal of Medicine publicou os resultados do estudo TRAVERSE, que avaliou a segurança do uso de testosterona em homens com mais de 45 anos com hipogonadismo. Este tópico revisa o tema e traz os resultados da publicação.
Gabapentinoides, Dor Neuropática e Eventos Adversos
Os gabapentinoides (pregabalina e gabapentina) são anticonvulsivantes amplamente utilizados para a dor neuropática. Vistos como drogas seguras, a prescrição dessas medicações têm aumentado progressivamente. Estudo publicado em julho no American Journal of Kidney Diseases (AJKD) investigou a associação de gabapentinoides e eventos adversos em idosos com doença renal crônica. Vamos ver os resultados e revisar a evidência sobre essas medicações.
Diretriz Americana de Insuficiência Cardíaca de Fração de Ejeção Preservada
O Colégio Americano de Cardiologia (ACC) lançou em 2023 uma diretriz sobre insuficiência cardíaca de fração de ejeção preservada (ICFEP). Esse documento faz parte de uma iniciativa para criação de diretrizes com abordagens práticas. Esse tópico resume as principais informações da publicação.
Herpes Simples
A infecção pelo herpes simples é comum e pode recorrer. Este tópico revisa a apresentação clínica, diagnóstico e tratamento das infecções pelos vírus do herpes simples HSV1 e HSV2.
