Caso Clínico #17
O caso clínico abaixo é apresentado em partes. O negrito é a descrição do caso, as partes que não estão em negrito são os comentários. Ao final, você encontrará a resolução e os pontos de aprendizagem resumidos.
Uma mulher de 38 anos procura o pronto-atendimento após início súbito de sudorese, calafrios, tremores em extremidades e palpitações. Os sintomas iniciaram no repouso, após o almoço. Nega dor precordial, dispneia, perda da consciência ou outros sintomas.
Informa episódios semelhantes nas últimas semanas, porém todos com recuperação espontânea. Também relata perda ponderal de 4 kg em um mês. Faz uso de levotiroxina 100 mcg para tratamento de hipotireoidismo e nega outros antecedentes patológicos ou uso de medicamentos.
Ao exame físico, apresentava pressão arterial de 134/88 mmHg, frequência cardíaca de 112 batimentos por minuto, frequência respiratória de 16 incursões por minuto, saturação de 98% em ar ambiente e temperatura axilar de 35,9 °C. Exames cardíaco e pulmonar sem alterações. Um eletrocardiograma realizado no pronto-atendimento mostrava taquicardia sinusal, sem outros achados. A glicemia capilar no momento do exame físico era de 38 mg/dL.
O relato é de um episódio de hipoglicemia sintomático em uma paciente previamente saudável. Esse não é um evento comum, diferente da percepção comum.
Hipoglicemia é um evento raro em pessoas que não recebem tratamento farmacológico para diabetes mellitus (DM). Apesar de divergências entre referências, um nível de glicemia sérica menor que 55 mg/dL é considerada hipoglicemia em pessoas não-diabéticas e saudáveis. Nessa população, abaixo desse limiar geralmente surgem sintomas.
Em pessoas com DM, o corte para considerar hipoglicemia é elevado para 70 mg/dL. Como essa população utiliza medicamentos com potencial de induzir hipoglicemia, níveis glicêmicos menores que 70 mg/dL mostram uma tendência à queda e devem alertar para o desenvolvimento de hipoglicemia sintomática. Na maioria dos casos, os eventos estão intimamente relacionados ao tratamento farmacológico do DM [1].
Os sintomas de hipoglicemia podem ser divididos em autonômicos e neuroglicopênicos. Sintomas autonômicos geralmente ocorrem em concentrações plasmáticas abaixo de 60 mg/dL, enquanto os sintomas neuroglicopênicos, em níveis abaixo de 50 mg/dL.
Sintomas autonômicos podem ser divididos em:
- Sintomas adrenérgicos: taquicardia, palpitação, tremores, ansiedade;
- Sintomas colinérgicos: sudorese, náusea, fome.
A presença de sintomas autonômicos e neuroglicopênicos é altamente sugestiva de hipoglicemia. As manifestações autonômicas são inespecíficas e podem mimetizar diversos quadros como doenças inflamatórias, desidratação, síncope vasovagal e abstinência de substâncias. Pessoas com sintomas autonômicos exclusivos, sem documentação de baixos níveis glicêmicos, muito provavelmente não apresentam um distúrbio hipoglicêmico.
É necessário sempre demonstrar a causalidade entre os sintomas apresentados e a ocorrência da hipoglicemia, evitando investigações desnecessárias em indivíduos saudáveis que não apresentam hipoglicemia verdadeira. A tríade de Whipple auxilia a firmar a causalidade dos sintomas durante a avaliação e consistente em:
- Sintomas compatíveis com hipoglicemia;
- Baixo nível de glicose plasmática;
- Resolução dos sintomas com a correção da glicemia.
A tríade de Whipple utiliza os níveis plasmáticos de glicose. Em muitos serviços, é comum o uso da glicemia capilar. Algumas situações clínicas podem falsear a aferição capilar, principalmente em situações de vasoconstrição periférica, como no choque hemodinâmico, uso de drogas vasoativas e fenômeno de Raynaud.
Em pacientes críticos, sépticos ou com disfunções orgânicas graves (principalmente renal e hepática), há perda de mecanismos protetores contra a hipoglicemia. Nesse caso, a hipoglicemia pode ser uma manifestação de disfunção orgânica.
Na paciente em questão, observa-se um quadro de hipoglicemia em paciente não diabético. O estado geral preservado, ausência de sinais de alarme e outros sintomas pesam contra alguma disfunção orgânica em curso. Os sintomas relatados são compatíveis com hipoglicemia e a paciente apresentava glicemia < 55 mg/dL. Contudo, para estabelecer a causalidade, os sintomas devem melhorar após a reposição. Antes da reposição, idealmente deve ser feita a coleta de glicemia plasmática para evitar os confundidores da glicemia capilar.
A paciente recebeu 40 ml de solução glicosada 50% endovenosa, apresentando melhora completa dos sintomas. A glicemia capilar 15 minutos após a reposição era de 124 mg/dL. A paciente negou novamente uso de medicamentos ou suplementos, bem como histórico de DM pessoal e familiar. Seu IMC era de 23 e não haviam alterações no exame físico.
Dado o histórico pessoal negativo e o episódio de hipoglicemia sintomática não provocado, a paciente foi mantida em observação no pronto-atendimento e realizada uma investigação inicial. A ingestão alimentar foi estimulada nesse período.
Os exames laboratoriais iniciais foram: glicemia plasmática de 118 mg/dL, Hb 13,2 mmHg, leucócitos 6.500/mm³ sem desvios, plaquetas 284.000/mm³, sódio 142 mEq/L, potássio 4,2 mEq/L, pH 7,42, bicarbonato de 21 mEq/L, lactato venoso de 11 mg/dL, ureia de 24 mg/dL e creatinina sérica 0,85 mg/dL. A paciente não apresentava alterações em enzimas hepáticas, bilirrubina total e albumina.
Ainda no período de observação, houve recorrência dos sintomas e uma nova glicemia capilar com resultado de 44 mg/dL, apesar da ingestão de alimentos e suplementação prévia. Uma glicemia plasmática foi coletada nesse novo episódio e confirmou a hipoglicemia.
A confirmação de glicemia plasmática < 55 mg/dL, associada aos sintomas compatíveis e a resolução após correção da glicemia preenchem os critérios da tríade de Whipple. Isso confirma que a paciente apresenta um distúrbio hipoglicêmico verdadeiro.
O primeiro passo após documentar uma hipoglicemia verdadeira é procurar por causas comuns dessa situação. Isso envolve revisar os medicamentos utilizados e buscar disfunções orgânicas.
Os exames laboratoriais afastam disfunções orgânicas agudas significativas. Na história não há evidência de uso de medicamentos ou substâncias que possam induzir o quadro.
Insulina ou secretagogos de insulina (como as sulfoniluréias) são os medicamentos mais associados com hipoglicemia e são a causa mais comum de hipoglicemia em pacientes diabéticos. Os principais medicamentos implicados em hipoglicemia estão resumidos na tabela 1.

O abuso de álcool pode predispor à eventos hipoglicêmicos por interação direta no metabolismo da glicose. O álcool também pode interagir com medicamentos que predisponham à hipoglicemia, aumentando o risco. Isso é especialmente importante se o paciente também for portador de doença renal crônica ou cirrose hepática.
A insuficiência adrenal pode causar hipoglicemia. Contudo, é incomum ocorrer hipoglicemia sem outras manifestações de insuficiência adrenal em adultos. Os exames laboratoriais também não sugerem essa causa. Veja mais na revisão sobre insuficiência adrenal.
Após afastar quadros sistêmicos e o uso de medicamentos/substâncias, o próximo passo é avaliar a presença de hiperinsulinismo levando à hipoglicemia. A tabela 2 resume os principais diagnósticos diferenciais de hipoglicemia no indivíduo não-diabético.
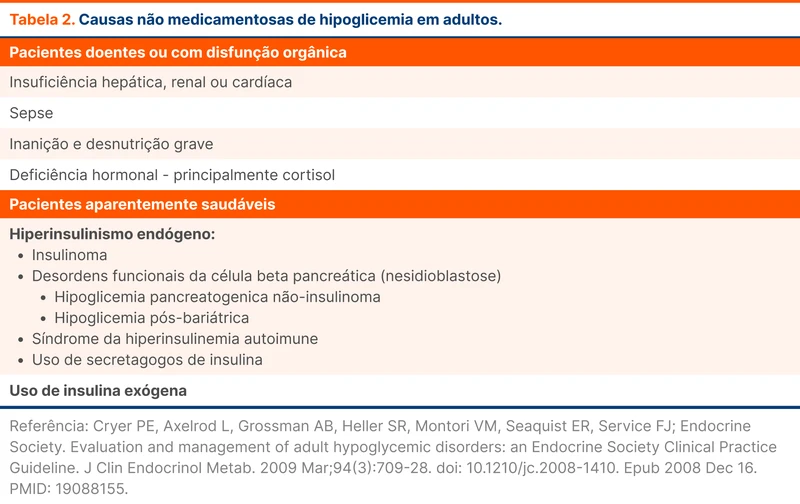
A investigação começa com a dosagem da insulina sérica, pró-insulina e peptídeo C durante o episódio hipoglicêmico. A dosagem da insulina aumentada confirma o hiperinsulinismo. A dosagem da pró-insulina e do peptídeo C auxiliam no diagnóstico diferencial entre hiperinsulinismo endógeno e exógeno.
A pró-insulina é um precursor da insulina, sendo clivada em insulina e peptídeo C. A relação esperada é de 1:1 entre insulina e peptídeo C. Porém, o peptídeo C apresenta maior meia-vida sérica que a insulina, o que torna seus títulos geralmente maiores do que os títulos de insulina. Se a dosagem do peptídeo C e da pró-insulina estão elevadas, confirma-se o diagnóstico de um distúrbio de hiperinsulinismo endógeno.
Em quadros auto-induzidos (transtorno factício ou síndrome de Munchausen) há uma administração de insulina exógena. Isso aumenta os níveis de insulina sérica e suprime a produção de insulina endógena. A manifestação laboratorial desse quadro é a redução dos níveis de peptídeo C e pró-insulina, indicando hiperinsulinismo exógeno.
Para uma investigação completa, também é recomendado a dosagem da cetonemia (geralmente de beta-hidroxibutirato) durante a hipoglicemia. Níveis baixos de beta-hidroxibutirato indicam que a atividade de insulina está inibindo a produção de cetonas, corroborando com o diagnóstico de hiperinsulinismo.
O teste da administração do glucagon é a última etapa da investigação. Se o paciente apresentar aumento da glicemia após a administração do glucagon, isso indica que os estoques hepáticos de glicogênio estão intactos, favorecendo o diagnóstico de hiperinsulinismo.
Caso não haja aumento com o teste do glucagon, entende-se que as reservas hepáticas estão consumidas. Isso sugere que há um componente de insuficiência hepática ou disfunção orgânica no episódio hipoglicêmico.
Alguns casos de suspeita de hiperinsulinismo endógeno podem ser um desafio diagnóstico. Caso o paciente não apresente eventos hipoglicêmicos espontâneos, existem protocolos de jejum supervisionados (48 a 72 h) ou testes de refeição mista (principalmente se os sintomas forem pós-prandiais) para tentar recriar condições de indução à hipoglicemia e permitir a avaliação laboratorial adequada.
Como a paciente não apresenta as principais causas de disfunção orgânica ou medicamentosa, está indicada a investigação aprofundada, preferencialmente durante um episódio hipoglicêmico.
A paciente foi admitida para investigação. Durante as primeiras 24 horas de internação, ocorreram outros dois episódios sintomáticos de hipoglicemia. Foi iniciada infusão contínua de solução glicosada a 5%.
No primeiro dia de internação, a paciente foi avaliada durante uma intercorrência por perda do nível de consciência. Na ocasião, apresentava glicemia capilar de 22 mg/dL. Dado a persistência de hipoglicemias sintomáticas, optou-se pela transferência para a UTI para vigilância e continuidade da investigação. Foi dosado o cortisol sérico matinal e ACTH, com resultados normais, descartando insuficiência adrenal.
Durante um episódio de hipoglicemia na UTI, foi realizada a investigação laboratorial aprofundada. A insulina sérica era de 122 nU/mL (VR < 3), o peptídeo C de 2 ng/mL (VR < 0,6) e a cetonemia sérica era negativa. Dado indisponibilidade no serviço, não foi realizado o teste de estímulo com glucagon.
Com a suspeita de de hiperinsulinemia endógena, uma tomografia de abdome com contraste foi solicitada para investigação de tumores pancreáticos ou outras anormalidades intra-abdominais. Não foram encontradas alterações relevantes na tomografia.
A paciente apresentou níveis elevados de insulina e peptídeo C e cetonemia negativa, confirmando o diagnóstico de hiperinsulinemia endógena.
Nesse ponto, é indicado a dosagem sérica de secretagogos de insulina (se disponível), para afastar a presença de distúrbios factícios por esse tipo de agente. A tabela 3 resume os principais padrões laboratoriais de eventos hipoglicêmicos, conforme cada etiologia.
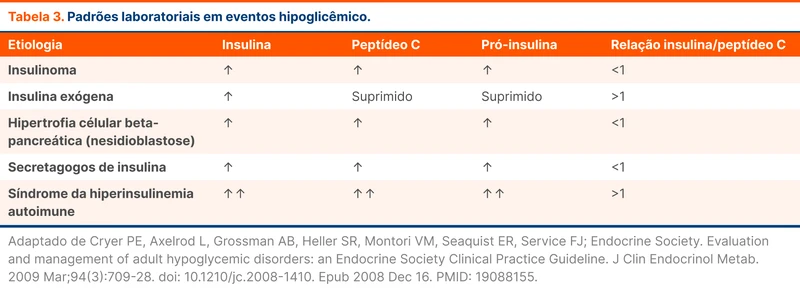
Dentre as causas de hiperinsulinemia endógena, duas merecem destaque: o insulinoma e a hipoglicemia pós-bariátrica [2].
O insulinoma é o tumor neuroendócrino funcionante mais comum do pâncreas. O paciente com insulinoma apresenta um quadro de hipoglicemia hiperinsulinêmica endógena. Após os exames de laboratório sugerirem este quadro, estudos de imagem como tomografia, ressonância e PET-CT são indicados na tentativa de localizar o tumor secretor e guiar o tratamento.
A hipoglicemia também pode se apresentar como complicação de cirurgias bariátricas, como o bypass gástrico e outros procedimentos que alteram a função do trato gastrointestinal alto. O mecanismo fisiopatológico não é bem estabelecido, bem como o tempo após a cirurgia que os sintomas ocorrem. A primeira linha de tratamento envolve modificações dietéticas, como fracionamento de refeições e dietas menos calóricas.
Para a investigação complementar da paciente, uma tomografia contrastada do abdome serve como rastreio inicial para pesquisa de insulinoma pancreático, que é a principal causa de hiperinsulinismo endógeno não medicamentoso.
O exame de imagem negativo indica a necessidade de investigação adicional. Nessa etapa uma hipótese que vale ser afastada é a de síndrome de hiperinsulinismo autoimune.
A dosagem de anticorpos anti-insulina resultou em altos títulos do anticorpo – 800 nU/mL (valor de referência 4-40) e foi realizado o diagnóstico de síndrome da hiperinsulinemia autoimune.
A paciente iniciou prednisona 1 mg/kg/dia, junto à dieta fracionada e com baixo teor de carboidratos. Após duas semanas do início do tratamento, não ocorreram novos episódios de hipoglicemia e teve alta hospitalar.
No seguimento ambulatorial, foi realizado desmame do corticoide. Mantiveram-se as recomendações dietéticas, não apresentando novos episódios de hipoglicemia sintomática.
A síndrome da hiperinsulinemia autoimune ou doença de Hirata é uma condição rara, mais frequente em pacientes de origem asiática. A síndrome decorre da produção de anticorpos contra a insulina endógena, em pacientes que não foram previamente expostos à insulina exógena e que não apresentam alterações anatomopatológicas no pâncreas [3].
A ligação dos anticorpos com a insulina torna a molécula ineficaz, o que costuma cursar com quadros de hiperglicemias pós-prandiais e estímulo para mais produção de insulina no pâncreas. Quando a produção de insulina supera a quantidade de anticorpos circulantes, os níveis glicêmicos começam a cair. É isso que explica os níveis extremamente elevados de insulina e peptídeo C.
O complexo insulina-anticorpo apresenta meia-vida sérica maior que a da insulina livre. Com o tempo, a ligação se enfraquece e ocorre liberação randômica da insulina do anticorpo. É nesse momento que a hipoglicemia ocorre, decorrente de uma liberação inapropriada de insulina em níveis glicêmicos normais.
Também em decorrência da maior meia-vida sérica do complexo, a relação insulina/peptídeo C tende a ser > 1. Esse cenário só é encontrado em outra situação clínica, o hiperinsulinismo exógeno (onde os níveis de peptídeo C encontram-se suprimidos). Na paciente em questão, a relação insulina/peptídeo C (com as unidades convertidas apropriadamente) era de 1.4.
A síndrome da hiperinsulinemia autoimune pode ser confundida com insulinoma ou outras condições de hiperinsulinismo endógeno, o que pode levar a exames/procedimentos invasivos desnecessários quando diagnóstico não é considerado [4].
Em até 80% dos pacientes, a remissão ocorre de maneira espontânea em 3-6 meses. A síndrome pode estar associada a outros distúrbios autoimunes ou até medicamentos.
A base do tratamento envolve o fracionamento de refeições com baixo teor de carboidratos para prevenir picos de insulina. A imunossupressão com corticoterapia pode ser utilizada em casos de hipoglicemias importantes, com o intuito de diminuir a titulação de anticorpos circulantes e auxiliar no controle glicêmico.
Alguns pontos de aprendizagem sobre o caso que você não pode esquecer:
- Hipoglicemia sintomática não é um evento esperado em indivíduos saudáveis sem tratamento medicamentoso para diabetes mellitus. Confirmar a tríade de Whipple é importante para estabelecer a causalidade da hipoglicemia com os sintomas do paciente.
- Disfunções orgânicas e distúrbios hormonais podem se manifestar com hipoglicemia. Esses quadros não necessitam de investigação adicional específica para hipoglicemia.
- Abuso de álcool ou medicamentos podem atuar como confundidores na avaliação. Distúrbios factícios também podem ser de difícil diagnóstico e devem ser suspeitados em indivíduos saudáveis com hipoglicemia.
- A investigação de hipoglicemia sem causa aparente começa com a dosagem da insulina sérica, pró-insulina e peptídeo C durante o episódio hipoglicêmico. A dosagem da insulina aumentada confirma o hiperinsulinismo. A pró-insulina e o peptídeo C ajudam a determinar se o excesso de insulina é endógeno ou exógeno.
- A síndrome da hiperinsulinemia autoimune é uma condição rara que cursa com produção de anticorpos anti-insulina e pode ser confundida com outros diagnósticos como insulinoma. A dosagem de anticorpos anti-insulina pode evitar exames complementares invasivos desnecessários no cenário de investigação de hiperinsulinismo endógeno. O tratamento é feito com adequação dietética e imunossupressão até melhora dos títulos dos anticorpos.
Aproveite e leia:
Insuficiência Adrenal
A adrenal é responsável por produzir glicocorticoides, mineralocorticoides e androgênios. Esta revisão aborda o diagnóstico e tratamento da insuficiência adrenal (IA), em pacientes estáveis e instáveis (crise adrenal).
Diabetes Mellitus e Drogas Antidiabéticas no Perioperatório
O controle glicêmico e o manejo de diabetes mellitus estão relacionados aos desfechos clínicos no perioperatório. Esse tópico aborda o manejo dessas condições no perioperatório.
Diretriz de Insuficiência Pancreática Exócrina
Insuficiência pancreática exócrina (IPE) pode ocorrer em diversas condições além da pancreatite crônica. Essa síndrome impacta a sobrevida e a qualidade de vida dos pacientes. Em novembro de 2023, a Associação Americana de Gastroenterologia publicou atualizações práticas sobre IPE. Este tópico aborda os principais aspectos de diagnóstico, manejo e acompanhamento.
Consenso de Emergências Hiperglicêmicas
Um novo consenso internacional de emergências hiperglicêmicas foi publicado em agosto do 2024 pela American Diabetes Association (ADA), European Association for the Study of Diabetes (EASD), American Association of Clinical Endocrinology (AACE) e outras sociedades. Publicado originalmente em 2001 e atualizado pela última vez em 2009, o documento agora incorpora os avanços mais recentes para o manejo dessas condições. Este tópico revisa aspectos práticos no diagnóstico e manejo da cetoacidose diabética e estado hiperglicêmico hiperosmolar.
Controle de Glicemia no Paciente Internado
Hiperglicemia hospitalar está associado a piores desfechos e maior risco de complicações. Em julho de 2024, a Sociedade Brasileira de Diabetes (SBD) publicou uma diretriz com recomendações práticas sobre hiperglicemia em pacientes não críticos no hospital. A Society of Critical Care Medicine (SCCM) também trouxe atualizações sobre metas e indicações do controle glicêmico no paciente crítico. Este tópico aborda o controle de glicemia no paciente internado.
