Terapia de Ressincronização Cardíaca na Insuficiência Cardíaca
A terapia de ressincronização cardíaca é uma das opções de tratamento da insuficiência cardíaca de fração de ejeção reduzida (ICFER). Em janeiro de 2024, o New England Journal of Medicine (NEJM) publicou os resultados de um estudo dessa terapia na ICFER. Este tópico revisa os principais dispositivos cardíacos eletrônicos implantáveis e o seu papel na ICFER [1].
Terapia de ressincronização cardíaca e outros dispositivos cardíacos eletrônicos implantáveis
A terapia de ressincronização cardíaca (TRC) é uma intervenção feita por um dispositivo cardíaco eletrônico implantável (DCEI). Além dos ressincronizadores, outros DCEI são os marcapassos (MP) e o cardiodesfibrilador implantável (CDI).
Os MP são usados para controle de ritmo especialmente em pacientes com bradiarritmias. A principais indicações são as seguintes:
- Doença do nó-sinusal;
- Bloqueio atrio-ventricular (BAV) do segundo-grau MOBITZ II;
- BAV avançado e BAV total (BAVT).
Existem MP com eletrodos apenas no ventrículo ou átrio direito (unicamerais) e MP com eletrodos nas duas câmaras direitas (bicamerais). Em geral, os MPs bicamerais são preferidos, principalmente por evitar o desenvolvimento da síndrome do marcapasso. Essa síndrome ocorre quando o estímulo gerado por um eletrodo ventricular é conduzido de maneira retrógrada para o átrio. Com o passar do tempo, a dissincronia átrio-ventricular pode levar à redução do débito cardíaco e congestão venosa (pulmonar e periférica).
Os ressincronizadores cardíacos possuem eletrodos biventriculares. Estão indicados no tratamento de pacientes com insuficiência cardíaca de fração de ejeção reduzida (ICFER), refratários à terapia farmacológica otimizada e com QRS alargado. A terapia farmacológica da ICFER pode ser revisada neste tópico do Guia. Com o alargamento do QRS, ocorre uma dissociação significativa entre a contração ventricular direita e esquerda. A ideia do estímulo biventricular é corrigir essa dissociação. O benefício do uso de ressincronizadores foi demonstrado na redução da mortalidade, ganho de qualidade de vida e melhora da função ventricular [2].
O CDI representa uma das terapias mais eficazes na prevenção de morte súbita de causas cardíacas. O CDI identifica a arritmia e administra de maneira autônoma uma carga elétrica com o intuito de desfibrilar o paciente. Estão indicados após um episódio de morte súbita abortada ou em pacientes de alto risco de arritmias ventriculares fatais. As indicações de CDI e TRC na ICFER são revisadas a seguir.
Indicações da TRC e do CDI na insuficiência cardíaca de fração de ejeção reduzida
Pacientes com ICFER podem continuar com sintomas e disfunção sistólica, mesmo com terapia farmacológica otimizada. Os fatores mais comuns relacionados à persistência dos sintomas são [3]:
- Insuficiência mitral moderada ou grave;
- Reserva funcional miocárdica reduzida;
- Dissincronia ventricular (secundária ao alargamento do QRS).
A estimulação biventricular da TRC tem o propósito de corrigir disfunções eletromecânicas na ICFER e melhorar o desempenho ventricular esquerdo. Quanto maior a duração do QRS, melhor é a resposta à TRC. Em relação ao tipo de dissincronia cardíaca, pacientes com bloqueio de ramo esquerdo (BRE) e duração do QRS > 150 ms são os que mais se beneficiam da TRC [4].
Poucos pacientes com bloqueio do ramo direito (BRD) foram incluídos nos estudos maiores, dificultando uma conclusão definitiva em relação aos efeitos da TRC nessa população. Em um estudo observacional, foi constatado pior desfecho em pacientes com BRD clássico [5].
Apesar da fibrilação atrial (FA) estar presente em 25% dos pacientes com IC, a maioria dos estudos que avaliaram o benefício da TRC excluiu pacientes com esta arritmia. Na FA o benefício da TRC é menor, principalmente pela dificuldade de controle da frequência cardíaca.
A morte súbita por arritmias ventriculares é uma das principais causas de óbito em pacientes com ICFER. Pacientes com ICFER e risco aumentado de morte súbita (cardiopatia isquêmica, fração de ejeção de ventrículo esquerdo < 35%) têm indicação de CDI para redução de mortalidade.
Muitos pacientes com indicação de CDI também se enquadram em critérios para TRC. Assim, a TRC pode ser indicada junto à implantação de CDI.
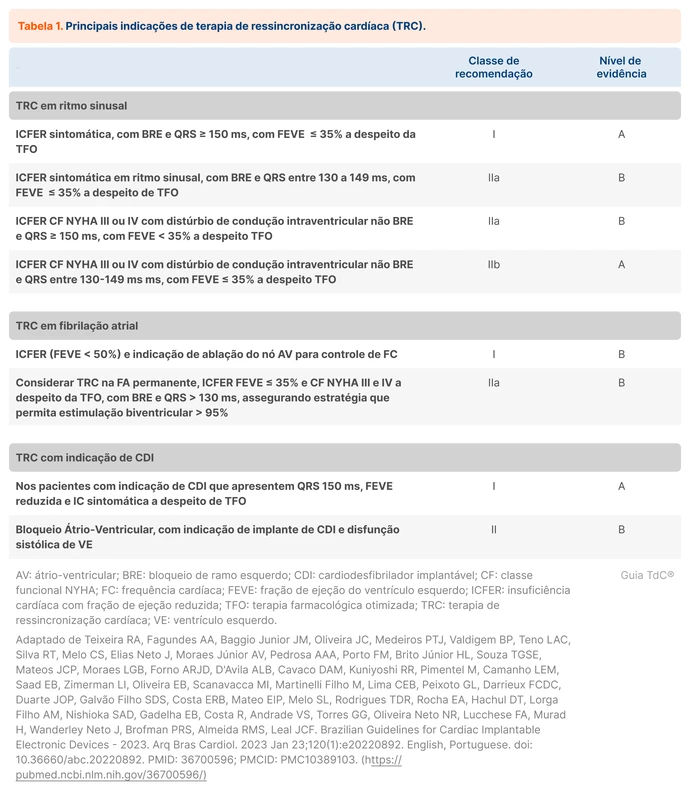
A tabela 1 e tabela 2 resumem as principais recomendações de TRC e CDI, conforme a Diretriz Brasileira de Dispositivos Cardíacos Eletrônicos Implantáveis de 2023 [3].

O estudo RAFT - uso de TRC e CDI na ICFER
O RAFT foi um estudo prospectivo, multicêntrico, duplo-cego e randomizado que avaliou o uso concomitante de TRC e CDI em pacientes com ICFER. Foram randomizados 1798 pacientes, com os seguintes critérios de inclusão [1]:
- ICFER NYHA classe II ou III
- Fração de ejeção de ventrículo esquerdo (FEVE) < 30% ou menos
- QRS > 120 ms (ou QRS de marcapasso > 200 ms)
- Ritmo sinusal
- Ritmo de FA/Flutter com frequência controlada ou planejamento de ablação do nó AV.
Todos tinham indicação e receberam CDI. Os participantes foram randomizados para implante concomitante de TRC (CDI+TRC) ou CDI isoladamente. O desfecho primário avaliado foi uma combinação de morte por qualquer causa ou internação por IC descompensada. Os desfechos secundários foram morte por qualquer causa, morte por causas cardiovasculares, além de internação por IC. O tempo de acompanhamento mediano foi de 40 meses.
Os resultados foram publicados em 2010, e demonstraram que a TRC associada ao CDI reduziu as taxas de morte e hospitalização por IC na população com IC leve-moderada. Houve maior incidência de eventos adversos relacionados ao dispositivo no grupo CDI+TRC (hemotórax e pneumotórax após implante e infecção relacionada ao dispositivo).
Os dados anteriores a esse estudo já haviam demonstrado benefício de diminuição de taxa de internação e melhora da qualidade de vida, mas em cenários de doença mais avançada (classe funcional III e IV) [6]. O benefício de mortalidade no RAFT foi mais evidente nos pacientes com classe funcional NYHA classe II. Na análise de subgrupo, os pacientes com QRS alargado (> 150 ms) tiveram maior benefício da combinação CDI associado à TRC.
A partir desses achados, esses pacientes foram incluídos nas recomendações de diretrizes para indicação de TRC.
Os resultados do acompanhamento prolongado foram publicados no NEJM em janeiro de 2024 [7]. Foram incluídos 1050 pacientes de oito dos principais centros de recrutamento do estudo RAFT. A média de idade da amostra foi de 66 anos, sendo 84% homens. O acompanhamento mediano geral foi de 7,7 anos e de 13,9 anos nos pacientes que sobreviveram.
O desfecho primário avaliado foi de morte por qualquer causa. O desfecho aconteceu em 405 dos 530 (76,4%) pacientes do grupo CDI, e em 370 dos 520 (71,2%) pacientes do grupo CDI+TRC. O tempo até a morte foi maior no grupo CDI+TRC.
O desfecho secundário foi um composto de morte por qualquer causa, transplante cardíaco ou implante de dispositivo de assistência ventricular esquerda. Os resultados também favoreceram o grupo CDI+TRC. O desfecho composto foi encontrado em 392 dos 520 (75,4%) pacientes, em comparação a 412 dos 530 (77,7%) pacientes do grupo CDI.
O benefício em relação à mortalidade manteve-se durante o período de acompanhamento. O desfecho composto secundário também mostrou redução no tempo até o evento, apesar das curvas de evento começarem a sinalizar uma convergência após 12 anos de seguimento.
Esses achados ocorreram mesmo com a inclusão de pacientes com menos ou nenhum benefício com esse tipo de intervenção em outros estudos (BRD, FA ou intervalo QRS 120-149 ms). A diferença entre os grupos também se manteve a despeito da ocorrência de diversas outras variáveis clínicas que podem impactar na sobrevida, como avanços no tratamento farmacológico, piora da doença e até disfunção do dispositivo.
Algumas limitações do estudo envolvem a alta taxa de mortalidade da população selecionada (aproximadamente 80% da amostra), além de mudanças importantes na terapia farmacológica que ocorreram durante o acompanhamento (como os inibidores da neprilisina e os inibidores da SGLT2). Além disso, apenas oito centros foram incluídos, e não o total da amostra originalmente avaliada.
O estudo contribui para consolidar o papel da TRC no tratamento da ICFER, demonstrando incremento em sobrevida, qualidade de vida e capacidade funcional. Também abre espaço para indicar a intervenção de maneira precoce em paciente com alargamento de QRS e redução da fração de ejeção ventricular esquerda, visando promover maior tempo de sobrevida com qualidade de vida [8].
Aproveite e leia:
Diretriz de Insuficiência Cardíaca AHA 2022
Em primeiro de abril foi divulgada a nova diretriz de Insuficiência Cardíaca (IC) da American Heart Association (AHA). O documento consolida várias descobertas recentes e traz nova ótica sobre pontos antigos. Aqui vão quatro tópicos de destaque do documento:
Diretriz de Doença Coronariana Crônica da AHA 2023
A doença coronariana crônica (DCC) tem um amplo espectro de manifestações. Em agosto de 2023 a American Heart Association (AHA) publicou uma diretriz com orientações sobre o manejo da DCC. Esta revisão traz as principais recomendações do documento.
Amiodarona
A amiodarona tem vários efeitos antiarrítmicos e é amplamente utilizada em taquiarritmias supraventriculares e ventriculares dentro e fora do hospital. Neste tópico revisamos seu mecanismo de ação, como prescrever e como evitar seus efeitos adversos durante a administração.
Estenose de Carótida Assintomática
Algumas diretrizes recomendam a revascularização de pacientes com estenose de carótida assintomática. Os estudos que demonstraram benefício com essa conduta são antigos, quando o tratamento clínico não era tão eficaz. Não sabemos se os resultados seriam os mesmos no contexto terapêutico atual. O SPACE-2, publicado no Lancet Neurology em outubro de 2022, foi desenhado para tentar tirar essa dúvida.
Novos Critérios Diagnósticos e Classificação da Obesidade
Uma nova proposta de critérios para o diagnóstico e classificação da obesidade foi publicada no Lancet em janeiro de 2025. Este tópico aborda essa nova publicação.
