Câncer de Reto e Inibidores de Checkpoint
As medicações antineoplásicas conhecidas como inibidores de checkpoint concederam o prêmio Nobel ao seus descobridores em 2018. Um estudo publicado no New England Journal of Medicine (NEJM) em junho de 2022 encontrou resultados animadores desses fármacos no manejo do câncer de reto [1]. Aproveitando a publicação, vamos rever o tema.
O que são inibidores de checkpoint
Inibidores de checkpoint são uma classe de antineoplásicos utilizada em várias malignidades diferentes. Essas medicações atuam nas vias que impedem que o sistema imune ataque o próprio corpo. As nossas células têm pontos de controle (checkpoints) que freiam os leucócitos, evitando um auto-ataque. Através desse mecanismo, algumas neoplasias superexpressam os checkpoints, dificultando a destruição das células neoplásicas pelo sistema imune.
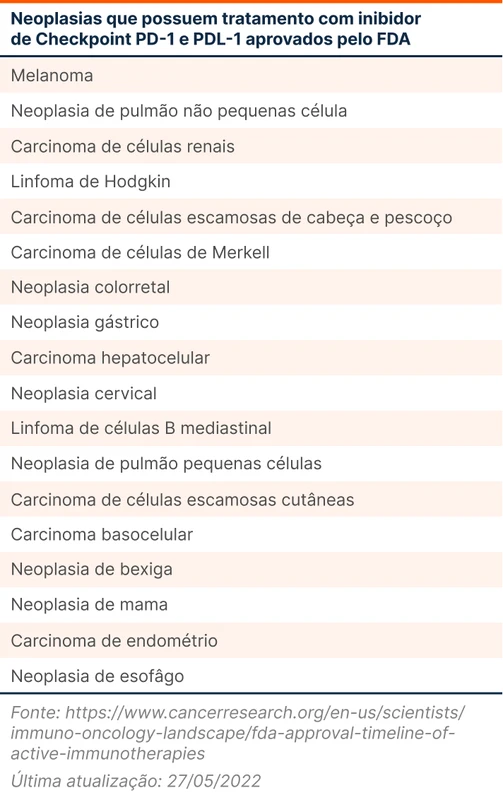
Um desses checkpoints é a PD1 (do inglês, programmed cell death protein 1). O seu bloqueio é um dos mais explorados, com aplicações para melanoma, neoplasia de pulmão não pequenas células e pequenas células, carcinoma urotelial e outros mais.
A Food and Drug Administration (FDA) aprovou algumas drogas inibidoras de PD-1:
- Pembrolizumabe (Keytruda)
- Nivolumabe (Opdivo)
- Cemiplimabe (Libtayo)
- Dostarlimabe (Jemperli)
Também estão disponíveis fármacos para outro checkpoint relacionado, o PD-L1 (do inglês, programmed cell death ligant protein 1):
- Atezolizumab (Tecentriq)
- Avelumab (bavencio)
- Durvalumab (Imfinzi)
Por que o estudo foi feito?
O adenocarcinoma de reto localmente avançado é tratado com uma estratégia multimodal, utilizando quimioterapia neoadjuvante e em seguida radioterapia e cirurgia. A resposta completa é atingida em 25% dos pacientes. Essa terapia traz consigo alguns efeitos adversos como incontinência urinária e fecal, infertilidade e até possíveis sequelas como necessidade de colostomia permanente.
Um subgrupo de neoplasias colorretais possui deficiência no reparo de incompatibilidade (mismatch) do DNA. Isso resulta em uma alta carga de mutações e instabilidade nos microssatélites (unidades de repetição do DNA). Esses pacientes têm menos resposta a quimioterapia e radioterapia. Ao selecionar apenas tumores de reto que apresentavam instabilidade de microssatélites, os inibidores PD1 apresentaram boa resposta em pacientes com metástase [2].
Na tentativa de otimizar a taxa de cura e minimizar efeitos adversos, esse estudo de fase 2 avaliou a resposta de pacientes com neoplasia de reto localmente avançado (estágios 2 e 3), mas sem metástase, ao inibidor de PD1 dostarlimab. Apenas pacientes com defeitos de reparo de mismatch foram incluídos.
Como foi feito o estudo e o que ele encontrou?
O protocolo do artigo envolve o uso inicial de dostarlimab, seguido de radioterapia associado com capecitabina, depois a ressecção cirúrgica. Caso o paciente apresentasse sinais clínicos, endoscópicos e radiológicos (ressonância magnética) de resposta clínica antes de alguma etapa do tratamento, a radioterapia ou a cirurgia eram suspensas.
Além de presença de metástases, foram excluídos pacientes que já receberam tratamento prévio e aqueles com escore ECOG (do inglês, Eastern Cooperative Oncology Group) maior ou igual a 2 (ver tabela 2). Considerando os efeitos colaterais do medicamento, também foram excluídos pacientes com doenças autoimunes, infecção ativa ou uso de outro imunossupressor nos últimos 7 dias.

Dezesseis pacientes foram selecionados para receber o medicamento, sendo que apenas 12 receberam o tratamento completo com dostarlimab por 6 meses. Os outros 4 ainda estavam recebendo o tratamento durante a publicação do estudo. Nesses 12 pacientes, a resposta clínica foi de 100%. Desses, nenhum chegou a realizar o resto do protocolo, não sendo feitas radioterapia ou cirurgia.
A medicação resolveu os sintomas de sangramento, constipação e dor abdominal de forma rápida: 81% dos pacientes apresentaram melhora completa em 9 semanas de tratamento. Não houve eventos adversos graves no período estudado.
O grande problema do estudo é seu tamanho muito reduzido. Contudo, esses resultados já são suficientes para motivar estudos maiores e multicêntricos. O tempo de seguimento também é uma questão, já que apesar de uma resposta satisfatória inicial, o tumor pode voltar a progredir após um período mais longo de seguimento.
Aproveite e leia:
Estado Hiperglicêmico Hiperosmolar e Outras Complicações Agudas do Diabetes
Em fevereiro de 2024, foi publicada uma coorte realizada na Dinamarca sobre estado hiperglicêmico hiperosmolar. Aproveitamos para rever as complicações agudas do diabetes e apresentar os dados do estudo.
Rastreio de Câncer de Mama: Novo Posicionamento da USPSTF
No final de abril de 2024, a United States Preventive Services Task Force (USPSTF), órgão responsável pelas recomendações de rastreio nos Estados Unidos, atualizou seu posicionamento sobre o rastreio do câncer de mama. Este tópico revisa o tema e traz a nova recomendação.
Diretriz ESMO de Neoplasia de Sítio Primário Desconhecido
Pacientes com câncer na maioria das vezes têm o sítio primário identificado. Há casos em que não se identifica a origem da neoplasia, uma situação chamada de câncer de sítio primário desconhecido. Em dezembro de 2022, foi publicada diretriz da European Society for Medical Oncology (ESMO) sobre o tema. Vamos revisá-la neste tópico.
Profilaxia Primária de Trombose no Paciente com Câncer
Pacientes com neoplasia possuem alto risco para desenvolvimento de eventos tromboembólicos. Encontrar o grupo que mais se beneficia de profilaxia primária é uma tema recorrente em diversos estudos nos últimos anos. O trabalho TARGET-TP, publicado na JAMA em novembro de 2023, propôs uma nova estratégia para identificar esses pacientes. Esse tópico revisa o tema e os resultados do estudo.
Tratamento da Hipercalcemia da Malignidade
A hipercalcemia é uma complicação de diversas neoplasias, determinando pior prognóstico. Uma diretriz sobre o manejo dessa complicação foi publicada pela Endocrine Society em dezembro de 2022 e aproveitamos para revisar as possibilidades terapêuticas.
