Hidroxiureia na Anemia Falciforme
Em setembro de 2022, foi publicada pela Cochrane uma metanálise avaliando a hidroxiureia na doença falciforme [1]. Aproveitando a publicação, vamos revisar o tema e avaliar o impacto desse estudo.
Anemia falciforme: por que ocorrem desfechos negativos?
A doença falciforme (DF) pode ser causada pela homozigose do gene da hemoglobina S (Hb SS), condição chamada de anemia falciforme (AF). A DF também pode ocorrer pela heterozigose do gene da hemoglobina S com outra variante da cadeia beta de hemoglobina - como a doença da hemoglobina S-beta-talassemia ou doença de hemoglobina SC.
Situações de menor oxigenação causam polimerização da Hb S, dando forma de foice para a hemácia. A hemácia falciforme tem maior adesão ao endotélio e menor flexibilidade.
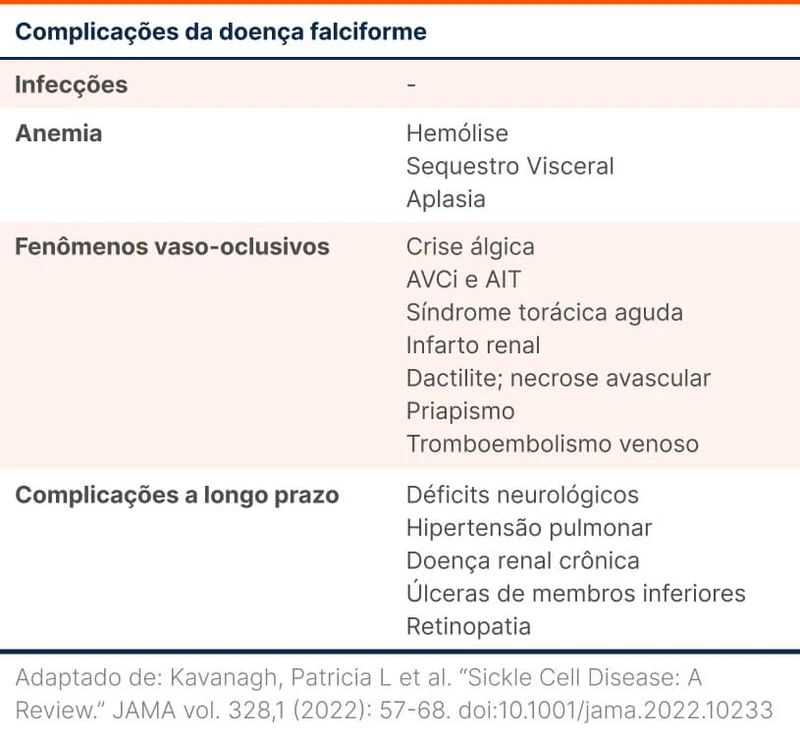
Essas alterações predispõem a vaso-oclusão, anemia hemolítica e outras complicações detalhadas na tabela 1. Na ausência de tratamento adequado, pessoas com DF têm menor sobrevida e diminuição da qualidade de vida [2].
Quais os tratamentos disponíveis para anemia falciforme?
A cura da AF no momento é possível apenas com o transplante de medula óssea. Essa é uma opção reservada para casos refratários. Estudos com terapia gênica são promissores [3].
Para a maioria dos pacientes, o tratamento se baseia em prevenção e manejo de complicações. No manejo entram os tratamentos para crises álgicas e síndrome torácica aguda por exemplo.
Na prevenção, um objetivo é reduzir infecções. As recomendações atuais priorizam o uso de penicilina profilática para crianças e atualização vacinal (focando na imunização contra microrganismos encapsulados - Neisseria meningitidis, Haemophilus influenzae, Streptococcus pneumoniae ) [4, 5]. Ainda na prevenção, a hidroxiureia tem papel relevante em reduzir crises álgicas.

O suporte transfusional tem muitas aplicações na AF. As indicações específicas estão detalhadas na tabela 2.
O papel da hidroxiureia
A hidroxiureia (HU) é um antineoplásico capaz de aumentar a hemoglobina fetal e a contagem de hemácias. Além disso, melhora o metabolismo de óxido nítrico e a interação das hemácias com o endotélio vascular [6].
Em setembro de 2022, a Cochrane revisou estudos que avaliaram o uso da hidroxiureia na DF, buscando desfechos como: controle de crise álgica, complicações graves (síndrome torácica aguda, sequestro visceral, AVC isquêmico) e mortalidade.
Os pesquisadores encontraram benefícios como redução da frequência de crises álgicas e aumento de hemoglobina fetal.
A metanálise não encontrou diferença significativa em relação à qualidade de vida, mortalidade e efeitos adversos graves da medicação - reforçando que a qualidade da evidência para esses desfechos é baixa.
A maioria dos estudos avaliou a população homozigótica (HbSS). As evidências para pessoas com heterozigose (HbSC, HbSβ+ ou HbSβº-talassemia) são geralmente extrapoladas dos estudos com homozigóticos. O tempo de seguimento dos estudos foi de no máximo 30 meses. Existe discussão quanto à segurança da medicação no uso a longo prazo.
Doses e efeitos adversos
Recomenda-se hidroxiureia para todos os indivíduos com AF.
A dose inicial é de 15mg/kg/dia para adultos, com alvo até a maior dose tolerada ou 30-35mg/kg/dia [7].
Efeitos adversos relatados incluem hiperpigmentação cutânea/ungueal, náuseas e diarreia. Os sintomas gastrointestinais podem ser melhor tolerados com fracionamento da medicação ou tomada noturna.
O efeito mielotóxico da hidroxiureia é dose-dependente, previsível e reversível. Seu uso necessita de monitorização com hemograma, especialmente quanto aos seguintes níveis:
- Neutrófilos: tolerar até 1500/mm³
- Plaquetas: tolerar até 80-150mil/mm³
- Reticulócitos: tolerar até 100.000/mm³
As evidências são conflitantes a respeito de infertilidade e teratogenicidade com o uso de hidroxiureia, tanto em homens quanto em mulheres. Muitas diretrizes recomendam métodos contraceptivos seguros ou interrupção do uso caso haja desejo de concepção.
Na doença renal crônica, sugere-se redução da dose [8].
Aproveite e leia:
Varfarina: Bulário e Quando Preferir em Relação aos DOACs
A varfarina é um anticoagulante antagonista da vitamina K. Ela atua inibindo os fatores de coagulação dependentes desse nutriente: proteína C, proteína S e fatores de coagulação II, VII, IX e X. Os anticoagulantes orais diretos (DOAC) são a primeira escolha em muitas situações, mas a varfarina ainda tem espaço na prática. Uma recente revisão do Journal of the American College of Cardiology avaliou essa questão e um ensaio clínico de janeiro de 2024 publicado no Circulation estudou a varfarina em indivíduos frágeis. Este tópico revisa o uso atual de varfarina.
Caso Clínico #7
Um homem de 65 anos com dispneia e cardiomegalia, evolui com hemorragia digestiva e hematomas.
Tromboembolismo no Paciente com Câncer
Em 2021 a American Society of Hematology publicou uma diretriz sobre tromboembolismo venoso (TEV) em pacientes com câncer. Um tema comum na prática hospitalar e ambulatorial. Vamos checar as principais recomendações.
Reposição de Ferro na Insuficiência Cardíaca
Pacientes com insuficiência cardíaca (IC) tem altas taxas de deficiência de ferro. Rastrear e tratar ferropenia em pacientes com IC pode levar a melhores desfechos. No congresso da American Heart Association (AHA) de novembro de 2022, foi publicado o estudo IRONMAN, que avaliou infusão de ferro intravenoso em pacientes com IC e ferropenia. Aproveitamos para revisar o tema neste tópico.
Caso Clínico #10
Homem de 38 anos com dispneia há 2 meses e eosinofilia.
