Diagnóstico e Erro Diagnóstico em Pneumonia Adquirida na Comunidade
Um estudo publicado no Journal of the American Medical Association (JAMA) Internal Medicine em março de 2024 evidenciou uma alta taxa de diagnósticos inapropriados de pneumonia adquirida na comunidade em pacientes hospitalizados [1]. Em agosto do mesmo ano, um artigo no Annals of Internal Medicine mostrou que mais da metade dos pacientes internados e tratados para pneumonia tem discordâncias entre o diagnóstico de admissão e o da alta [2]. Este tópico aborda o diagnóstico e os erros diagnósticos de pneumonia adquirida na comunidade.
Diagnóstico de pneumonia adquirida na comunidade e sinais clínicos
Não existe um padrão ouro para o diagnóstico de pneumonia adquirida na comunidade (PAC). Muitos estudos de PAC usam uma definição de pneumonia que envolve a combinação de sinais e sintomas com uma opacidade radiográfica sugestiva de processo inflamatório no parênquima pulmonar. Esse critério é inespecífico e pode ser o resultado de muitas outras condições cardiopulmonares.
Uma dúvida comum é quando solicitar uma radiografia de tórax para averiguar a possibilidade de PAC em um paciente com sintomas respiratórios agudos. O estudo 3C avaliou essa questão, recrutando pacientes com tosse aguda e utilizando a radiografia alterada como padrão para o diagnóstico [3]. De um total de 28.800 pacientes, 720 levaram o médico a solicitar uma radiografia e 115 tinham pneumonia pela imagem (16% dos 720). Esses dados fornecem uma noção da probabilidade basal de pneumonia nos pacientes com tosse aguda. Febre, estertores, hipoxemia (saturação menor que 95%) e taquicardia se correlacionam com pneumonia, mas de maneira fraca. A presença desses quatro achados ao mesmo tempo teve valor preditivo positivo de apenas 57%.
A dificuldade de estimar a probabilidade de PAC baseando-se apenas em anamnese e exame físico é conhecida há muito tempo [4]. Estudos mais recentes podem ajudar nessa estimativa. Sinais vitais normais e exame físico pulmonar normal juntos tem uma razão de verossimilhança (RV) negativa de 0,1, tornando pneumonia bastante improvável [5]. A impressão clínica geral do médico é útil para sugerir pneumonia, com RV positiva de 7,7, porém não ajuda a descartar, com RV negativa de 0,5 [6]. Sinais individuais ajudam pouco e o médico não deve utilizar a ausência de um achado, como estertores pulmonares, para descartar PAC [7].
A proteína C reativa pode ajudar em casos de dúvida. Se for usada como uma variável dicotômica, o corte de 30 mg/L parece ser o ideal, com valores acima disso sugerindo PAC [8]. Vários escores clínicos já foram elaborados para PAC, porém não parecem superar a impressão clínica e alguns carecem de validação [7, 8].
A baixa correlação entre o quadro clínico e os achados de imagem é um dos motivos para a diretriz de 2019 considerar apenas estudos com confirmação radiográfica do quadro [9]. Apesar disso, o diagnóstico operacional de pneumonia pode ser feito sem a imagem, para dar andamento a medidas mais urgentes, mas um exame de imagem está sempre recomendado se estiver disponível [10].
Exames de imagem
A radiografia de tórax em incidência póstero-anterior e lateral é o exame de imagem inicial para a maioria dos pacientes com suspeita de PAC. A radiografia é um método barato, acessível e rápido, sendo suficiente para a maioria dos pacientes.
É comum ter incerteza na avaliação da radiografia. Estudos mostram variabilidade na interpretação dos achados entre radiologistas [11, 12] e entre médicos da emergência e os radiologistas [13]. Em pacientes hospitalizados, parece existir uma tendência de sobrediagnóstico de PAC na interpretação da radiografia por médicos da emergência [14]. Isso deve ser considerado em pacientes recém-admitidos do pronto-socorro, especialmente quando o quadro clínico deixa dúvidas. O sobrediagnóstico de PAC em pacientes que vão ser admitidos pode ser explicado pela pressão para administração precoce de antibióticos, necessidade de tomar decisões rápidas e sobrecarga de trabalho no pronto-socorro.
Apesar da alta sensibilidade da tomografia computadorizada (TC), não existe evidência de que o uso rotineiro seja benéfico. O uso indiscriminado pode levar a custos elevados, longas esperas por resultados e exposição desnecessária à radiação. Segundo o Colégio Americano de Radiologia, a TC é apropriada após uma radiografia negativa ou duvidosa em pacientes com uma doença respiratória aguda com exame físico sugestivo, alteração de sinais vitais, doença neurológica central (que compromete a anamnese e exame físico) e outros fatores que aumentem o risco de desfecho desfavorável. Entre esses fatores estão idade avançada, comorbidades significativas e dificuldade no acompanhamento clínico ambulatorial. Outra indicação é a suspeita de complicações melhor avaliadas por TC, como derrame parapneumônico e abscesso [15].
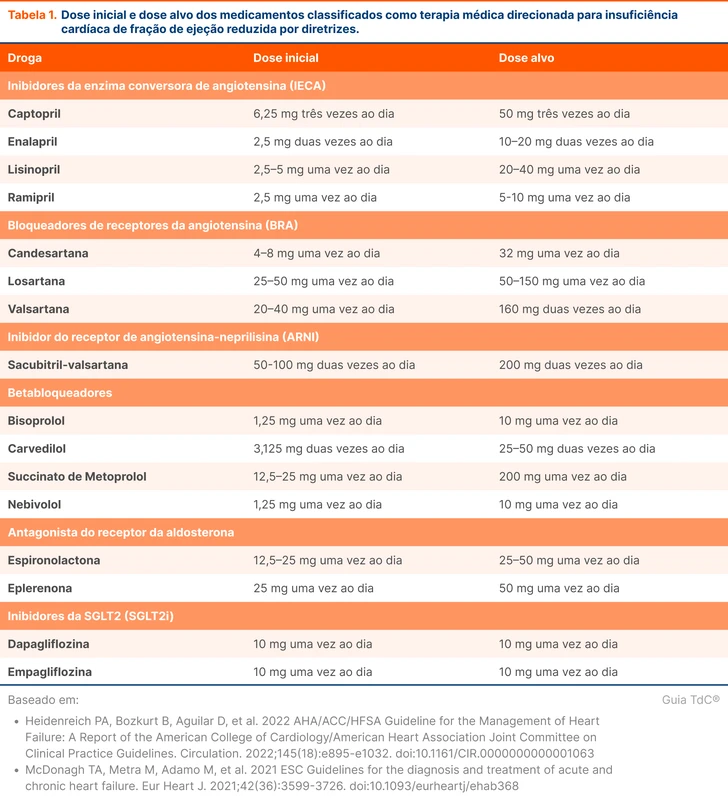
A tabela 1 agrupa cinco potenciais indicações de TC na suspeita de PAC. Quando a suspeita de PAC permanece apesar de uma radiografia sem achados convincentes, a TC não está disponível e o paciente vai ser internado, é razoável tratar empiricamente e repetir uma radiografia em 24 a 48 horas [16].

Vários estudos recentes reforçam a utilidade da ultrassonografia no diagnóstico de PAC [17, 18]. O desempenho do método varia conforme a habilidade do profissional com o aparelho. Uma aplicação é em pacientes instáveis com radiografias adquiridas no leito, muitas vezes com qualidade inferior e achados duvidosos, quando a TC não está disponível ou o paciente não tem condições de transporte.
Erro diagnóstico e diagnóstico diferencial
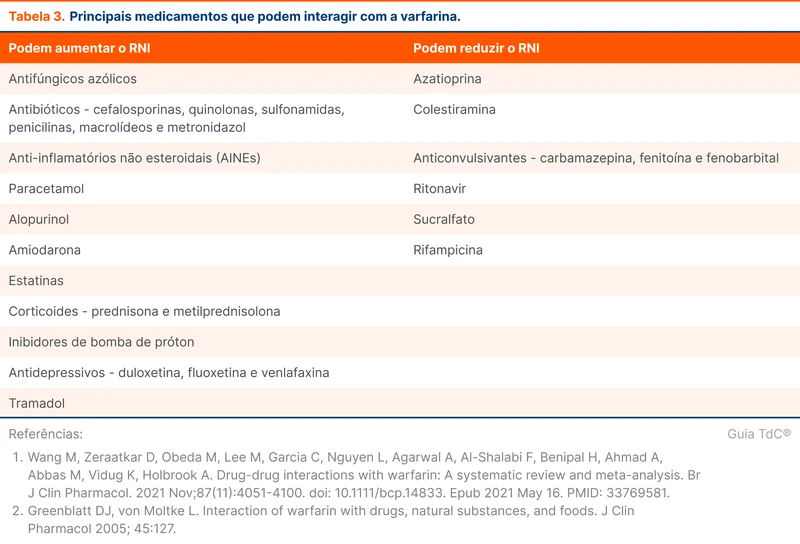
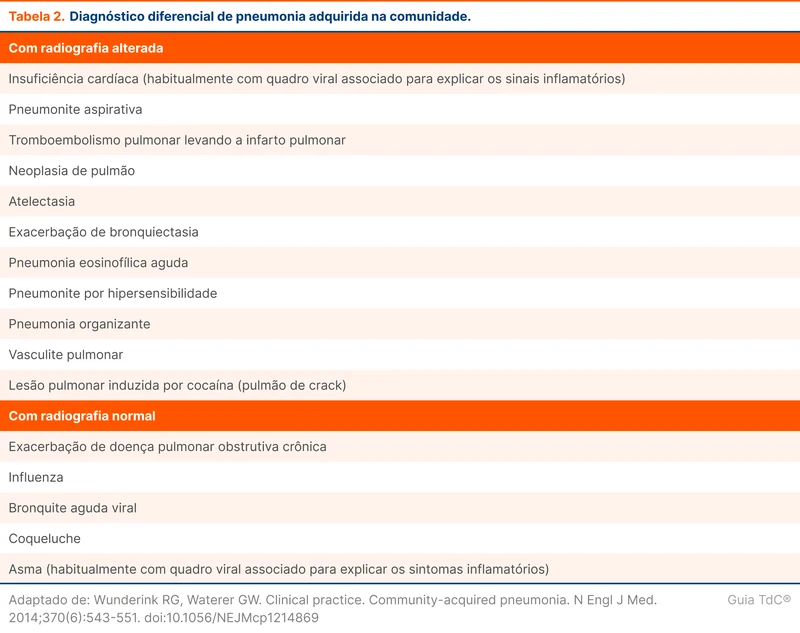
Erros diagnósticos envolvendo PAC podem prejudicar os pacientes por atraso no diagnóstico e exposição desnecessária a antibióticos. O diagnóstico tende a ser mais difícil em pacientes idosos com doenças cardiopulmonares de base. A tabela 2 organiza os diagnósticos diferenciais conforme a presença de opacidades na radiografia.
Um estudo recente publicado no JAMA Internal Medicine avaliou 17.290 pacientes internados que tiveram PAC como diagnóstico de alta hospitalar [1]. Via revisão de prontuário, os pesquisadores buscaram aqueles que receberam o diagnóstico inapropriado. Para isso, utilizaram uma métrica endossada pela National Quality Forum, que considera inapropriado qualquer tratamento antibiótico para PAC em um paciente que tenha menos que dois sinais ou sintomas ou que não tenha um achado radiográfico compatível [19]. O diagnóstico foi considerado inapropriado em 2079 pacientes, 12% do total. Pacientes com diagnóstico inapropriado tinham idade mais avançada, demência e alteração do estado mental na apresentação.
Outro estudo publicado no Annals of Internal Medicine examinou achados radiográficos e a concordância entre o diagnóstico de admissão e de alta envolvendo PAC [2]. Foram avaliados 317 mil internações que tiveram o diagnóstico de PAC em algum momento. Entre aqueles com diagnóstico de alta de pneumonia e com imagem alterada, 33% não tinham esse diagnóstico na admissão. Esses pacientes tiveram maior mortalidade, uma possível consequência do atraso de tratamento.
Já entre os inicialmente diagnosticados com PAC, 36% tiveram alta com outro diagnóstico e 21% não tinham alterações radiográficas compatíveis. Esses achados sugerem que uma análise cuidadosa das imagens pode reduzir o sobrediagnóstico de PAC. Uma expressão da incerteza diagnóstica é o fato que 10% dos pacientes receberam três tratamentos (antibiótico, corticoide e diurético) nas primeiras 24 horas. Mais da metade dos pacientes tiveram discordância entre o diagnóstico de PAC da admissão e da alta.
Os estudos ilustram a dificuldade e imprecisão diagnóstica de PAC. Mesmo com a maior disponibilidade de TC e métodos moleculares, o problema persiste. Uma parte dessa questão é inevitável, considerando a apresentação indiferenciada de muitos pacientes. Por outro lado, o acompanhamento evolutivo e a revisão dos exames complementares pode garantir um cuidado mais preciso.