Rastreio de Câncer de Próstata
Um assunto muito debatido na literatura urológica é o rastreio de câncer de próstata. Neste tópico, trazemos o estudo GÖTEBORG-2 que avaliou o uso da ressonância magnética para selecionar a indicação de biópsias de próstata. Aproveitamos e revisamos o tema [1].
Quem poderia se beneficiar do rastreio de câncer de próstata?
O câncer de próstata é a segunda maior causa de morte por câncer entre homens no Brasil. Apesar de ser um câncer muito prevalente, a letalidade não é alta em comparação com outras neoplasias [2].
Estudos de autópsia indicam que até 30% dos homens com 50 anos e 70% dos homens com 70 anos têm câncer de próstata. Na maior parte das vezes, essas neoplasias não haviam sido identificadas em vida. Esses dados sugerem que o risco de sobrediagnóstico é alto [3].
Uma revisão da Cochrane de 2018 investigou o rastreio do câncer de próstata [4]. Incluindo 5 ensaios clínicos randomizados com mais de 720 mil homens, o estudo encontrou que o rastreio se associa a um maior número de diagnósticos de câncer e detecção de doenças menos avançadas, mas sem benefício de sobrevida.
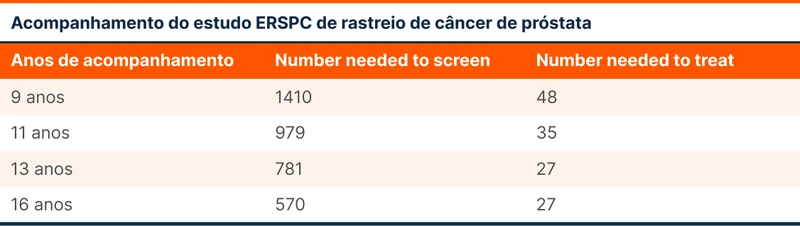
O estudo ERSPC incluiu mais de 180 mil homens e viu uma diferença significativa de mortalidade por câncer devido ao rastreio a cada 2 a 4 anos [5]. O protocolo incluiu homens de 50 a 74 anos e indicava biópsia de próstata caso o PSA fosse maior do que 3 ou 4 ng/mL (o valor de corte dependia do centro). Os pacientes deste estudo seguem sendo acompanhados e o NNT está caindo ao longo do tempo, indicando que o benefício se amplia de acordo com a sobrevida dos pacientes, conforme indica a tabela 1. Segundo os dados deste estudo, o rastreio sistemático pode reduzir a mortalidade, mas com sobrediagnóstico.
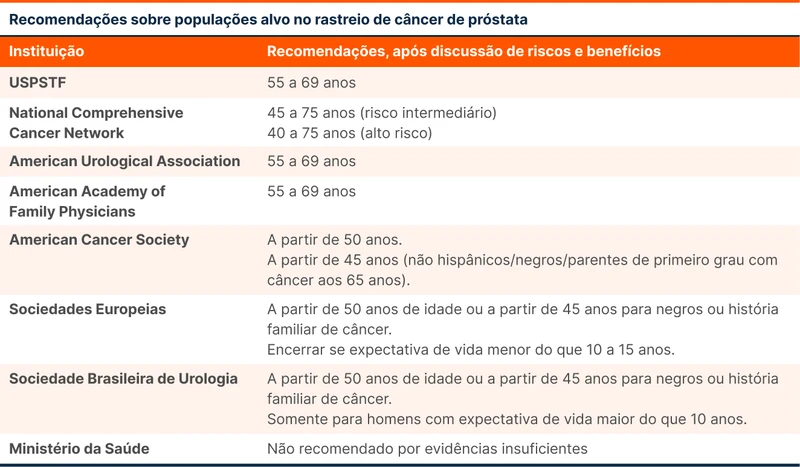
A USPSTF considera que o tratamento do câncer em estágio inicial detectado por rastreio provavelmente diminui a chance de progressão clínica e de doença metastática e talvez reduza a mortalidade. A tabela 2 traz recomendações sobre as populações alvo que poderiam se beneficiar com o rastreio do câncer de próstata [6-8, 9].
Como conversar com o seu paciente sobre o rastreio?

A Cartilha do INCA simplifica a discussão em 2 tópicos sobre benefícios e 2 sobre os riscos do rastreio de câncer de próstata (tabela 3) [10]. Outra maneira de conversar sobre o rastreio é trazendo dados dos grandes estudos, como na tabela 4, traduzida do documento da USPSTF.
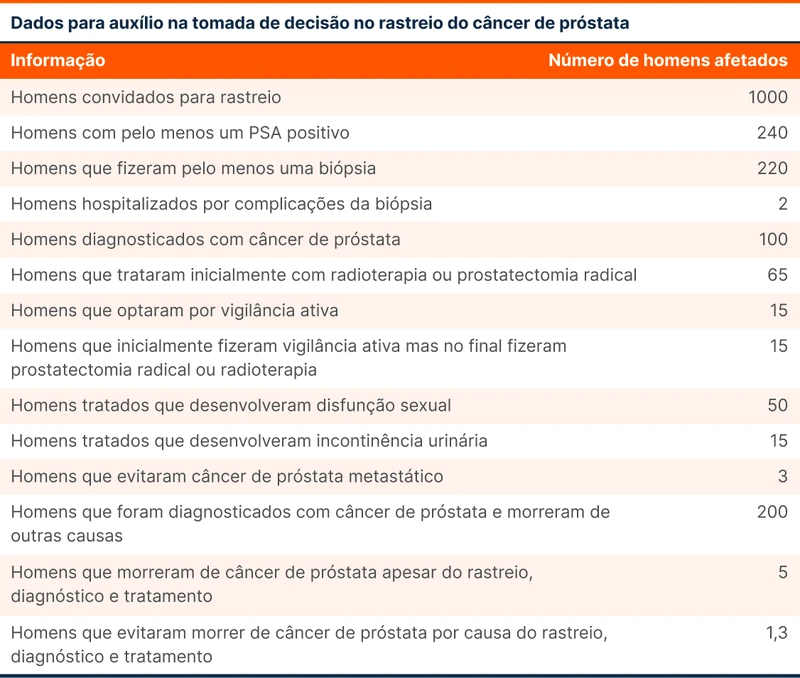
Como fazer o rastreio?
O rastreio deve ser feito com a dosagem de PSA. A USPSTF não recomenda o toque retal, considerando que a maior parte dos trabalhos excluiu esse exame e não existe evidência de benefício [6]. Já a diretriz europeia de urologia recomenda PSA e toque retal, pois acredita que a baixa acurácia nos diagnósticos ocorre na atenção primária provavelmente por inexperiência dos examinadores [11].
Quanto maior o valor do PSA, maior é o risco de câncer de próstata e de cânceres mais agressivos. Nos Estados Unidos, PSA > 4 ng/mL é indicação de biópsia. Já na Europa, quando PSA > 3 ng/mL indica-se a biópsia.
O maior problema do rastreio é o diagnóstico de cânceres de baixo risco e as complicações relacionadas ao tratamento. Isso ocorre pela alta prevalência de cânceres de próstata indolentes, de crescimento lento ou que não progridem [6].
Quatro estratégias podem diminuir os malefícios relacionados ao rastreio:
- Identificar pacientes de grupos de risco
- Individualizar o intervalo de um novo teste - Pacientes com PSA < 1 ng/mL e 40 anos de idade ou < 2 ng/mL e 60 anos de idade podem adiar a repetição do PSA em até 8 anos.
- Melhorar as indicações da biópsia usando calculadoras de risco ou ressonância magnética (RM) - As calculadoras de risco devem ser adequadas à população estudada. A coorte ERSPC gerou a seguinte calculadora e na coorte PCPT foi utilizada esta segunda ferramenta.
- Biópsias guiadas e aplicação de vigilância ativa para doenças de baixo risco.
O que o estudo pode mudar no rastreio?
O estudo GÖTEBORG-2 utilizou a ressonância magnética para tentar melhorar as indicações de biópsia e para guiar o procedimento da biópsia.
Dezoito mil homens de 50 a 60 anos foram randomizados em dois grupos. Todos os participantes faziam rastreio com PSA e realizavam RM se PSA > 3 ng/mL. O grupo intervenção ia para biópsia guiada apenas se houvesse uma lesão PI-RADS 3 ou mais ( escala radiológica que vai de 1 a 5 que indica o grau de suspeição da lesão). O grupo de referência realizava biópsia independente dos achados da RM. Todos os pacientes com PSA acima de 10 ng/mL eram biopsiados, independentemente dos resultados da RM.
Menos pacientes do grupo intervenção tiveram diagnóstico de câncer de próstata clinicamente insignificante, em comparação com o grupo de referência. A incidência de câncer de próstata clinicamente insignificante foi de 0.6% no grupo da biópsia guiada e 1.2% no grupo da biópsia sistemática, uma diferença de -0.7% (95% IC -1,0 a -0.4; risco relativo, 0.46; 95% IC, 0.33 a 0.64; P < 0.001). Não houve diferença significativa no diagnóstico de câncer clinicamente significativo.
O critério de câncer clinicamente insignificante foi a escala de Gleason 3+3 ou ISUP 1. Dez pacientes foram diagnosticados com cânceres clinicamente significativos que não foram vistos na RM. Seis desses pacientes fizeram vigilância ativa (não houve intervenção).
Introduzir a RM antes da biópsia em pacientes com PSA entre 3 e 10 poderia reduzir pela metade o risco de detecção de cânceres insignificantes. Essa estratégia pode reduzir o número de biópsias e suas complicações, com um custo de perder um número pequeno de cânceres clinicamente significativos.
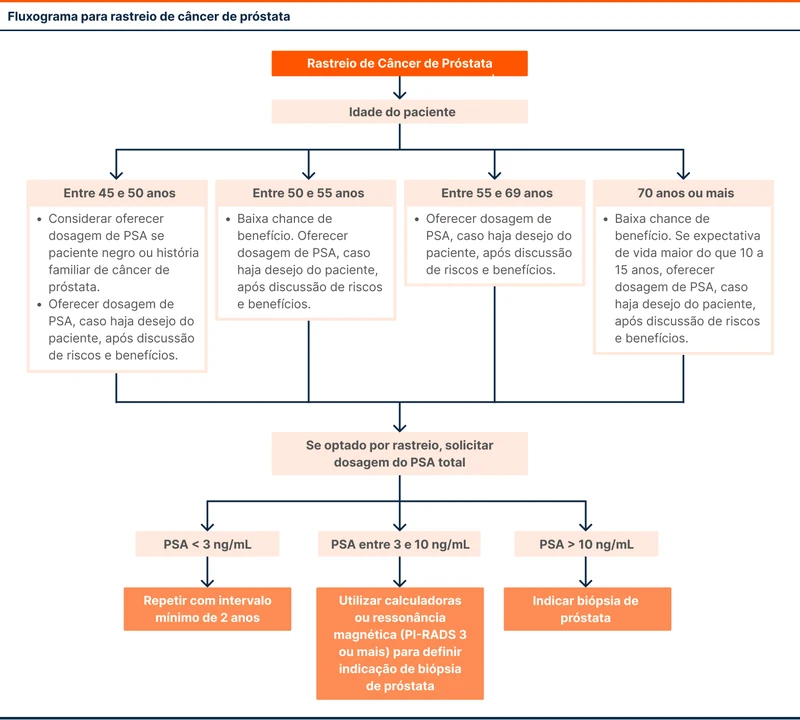
O fluxograma 1 traz uma sugestão de como fazer o rastreio do câncer de próstata.