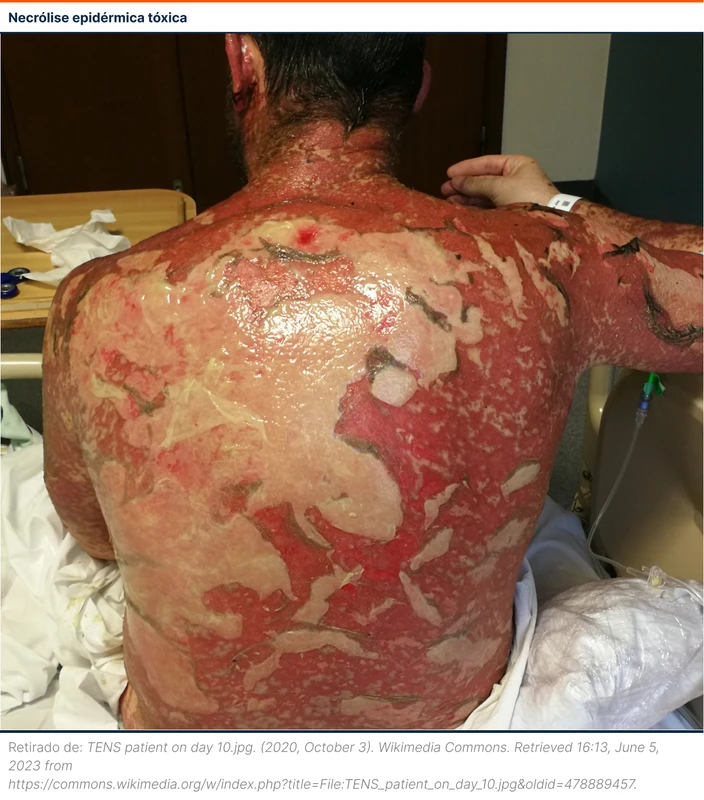
Etomidato na Intubação de Sequência Rápida
O etomidato é um dos sedativos mais utilizados na intubação por ter uma ação rápida e relativa estabilidade hemodinâmica. Em abril de 2023, foi publicada no Journal of Critical Care uma meta-análise comparando o etomidato contra outros sedativos em intubação de pacientes críticos [1]. Este tópico revisa o uso de etomidato na intubação e traz os resultados do novo estudo.
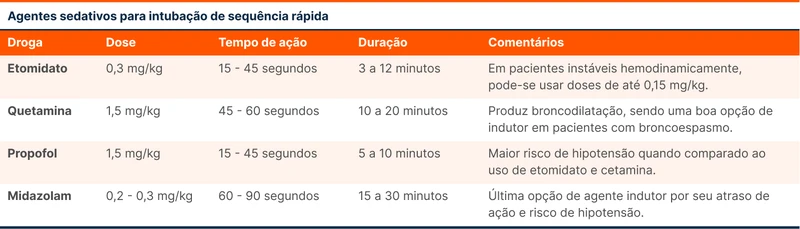
Agentes sedativos na intubação de sequência rápida
Em pacientes críticos, todos os agentes sedativos para intubação podem causar hipotensão.
A instabilidade hemodinâmica ocorre em até 42% dos pacientes críticos que precisam ser intubados. Cerca de 90% dos pacientes com essa complicação precisam iniciar ou aumentar a dose de vasopressores durante o procedimento. A ocorrência de instabilidade hemodinâmica está associada à mortalidade [2].
Os agentes sedativos devem ter um início de ação rápido (em até 60 segundos), induzindo inconsciência. Os medicamentos mais disponíveis para sedação são etomidato, quetamina, propofol e midazolam (veja tabela 1). Esses sedativos são altamente lipofílicos, cruzando a barreira hematoencefálica rapidamente e agindo em segundos.
Houve uma redução significativa no uso do midazolam nas últimas décadas, atualmente considerado como opção apenas quando outros agentes não estão disponíveis. O midazolam é comumente subdosado na intubação de emergência e pode causar hipotensão significativa em doses habituais (0,2 a 0,3 mg/kg) [3]. Para evitar esse efeito colateral, muitas vezes doses menores são feitas, o que pode lentificar o início de ação e reduzir a profundidade da sedação.
De acordo com os registros NEAR, o etomidato é o medicamento mais utilizado atualmente. Sua ação rápida e relativa estabilidade hemodinâmica em comparação com os outros agentes explicam essa tendência.
Uso do etomidato na intubação de sequência rápida
O etomidato é um derivado imidazólico que possui efeito hipnótico, mas sem efeito analgésico. Sua ação ocorre através da potencialização da atividade do neurotransmissor GABA.
O etomidato é visto como o sedativo mais estável do ponto de vista cardiovascular entre as opções disponíveis [4-6]. Também é considerado uma boa escolha na intubação de pacientes com hipertensão intracraniana. O medicamento atenua o aumento da pressão intracraniana e preserva a estabilidade hemodinâmica durante o procedimento.
A dose usual é de 0,3 mg/kg. Em pacientes instáveis, uma dose de 0,15 mg/kg pode ser suficiente para gerar hipnose adequada enquanto tenta-se manter a estabilidade.
O etomidato causa inibição reversível da produção de cortisol através do bloqueio da enzima 11-beta-hidroxilase. Esse efeito é mais intenso durante a infusão contínua, modo de administração em que não é mais indicado [7]. Por conta desse mecanismo, seu uso no paciente crítico é debatido, especialmente na sepse. As evidências atuais não são definitivas sobre essa questão, com poucos estudos randomizados com baixo risco de viés sobre o assunto [8, 9]. Uma meta-análise de ensaios clínicos com pacientes críticos gerais, não apenas sépticos, não evidenciou aumento de mortalidade com o uso da droga [10].
Um dos ensaios clínicos randomizados mais recentes foi o EvK de 2022 [11]. Esse estudo foi realizado em um centro único dos Estados Unidos comparando etomidato com quetamina em pacientes críticos. Os resultados mostraram maior sobrevida em sete dias com a quetamina, um benefício que não se manteve com 28 dias. O poder do estudo foi adequado, mas é difícil generalizar os resultados pelo alto risco de viés:
- O time responsável pela via aérea poderia ter excluído pacientes que não foram excluídos pelo protocolo.
- Os clínicos assistentes não estavam cegados, o que significa que sabiam qual tratamento estava sendo administrado. Os pacientes do grupo quetamina receberam mais vasopressores, o que pode ter influenciado na taxa de mortalidade precoce em sete dias.
- A avaliação dos desfechos também não foi cegada, ou seja, os avaliadores sabiam qual tratamento cada paciente recebeu.
O que a nova meta-análise evidenciou?
A revisão sistemática e meta-análise em questão incluiu onze ensaios clínicos, entre eles o estudo EvK de 2022. A intervenção avaliada foi uso de etomidato contra qualquer outra droga sedativa na intubação de doentes críticos adultos. O desfecho primário avaliado foi mortalidade.
A meta-análise encontrou um aumento de mortalidade com o uso de etomidato (23% vs. 20%; RR 1,16; IC 95% 1,01 - 1,33). Quando comparado exclusivamente à quetamina, o resultado se manteve.
Dos onze ensaios clínicos incluídos, três contribuíram com a maior parcela da população avaliada. O estudo EvK teve um peso de 21%, sendo o estudo que mais impactou no resultado evidenciado pela meta-análise. Ainda assim, o intervalo de confiança ficou bem próximo de 1.
Esta não é uma evidência definitiva contra o uso de etomidato, mas levanta uma preocupação. O etomidato continua sendo uma opção na intubação de sequência rápida, principalmente em pacientes hipotensos quando as outras opções são propofol e midazolam. A quetamina é uma boa escolha neste contexto de dúvida na literatura, especialmente em pacientes com choque séptico.