Tomografia de Crânio no Delirium
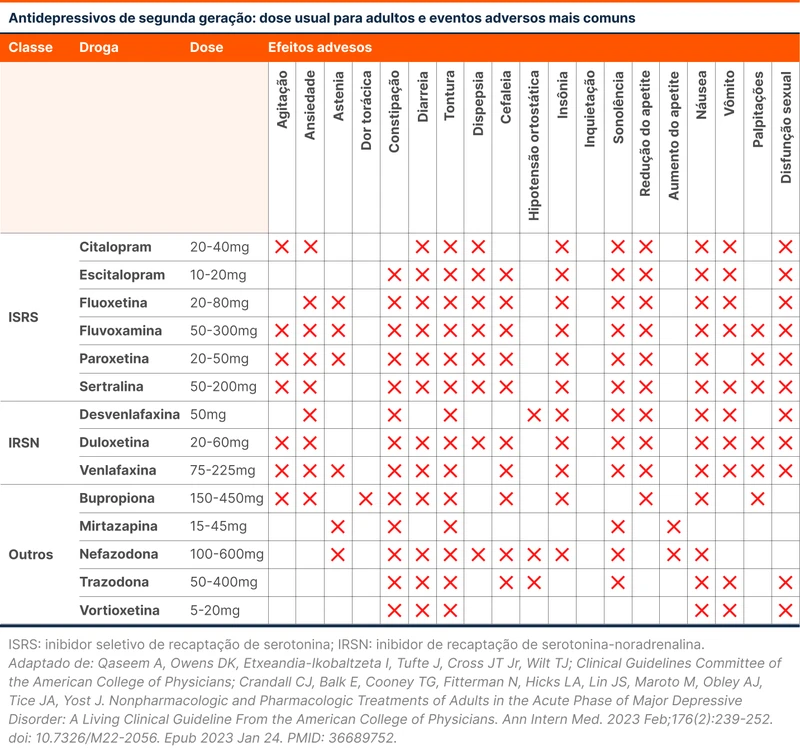
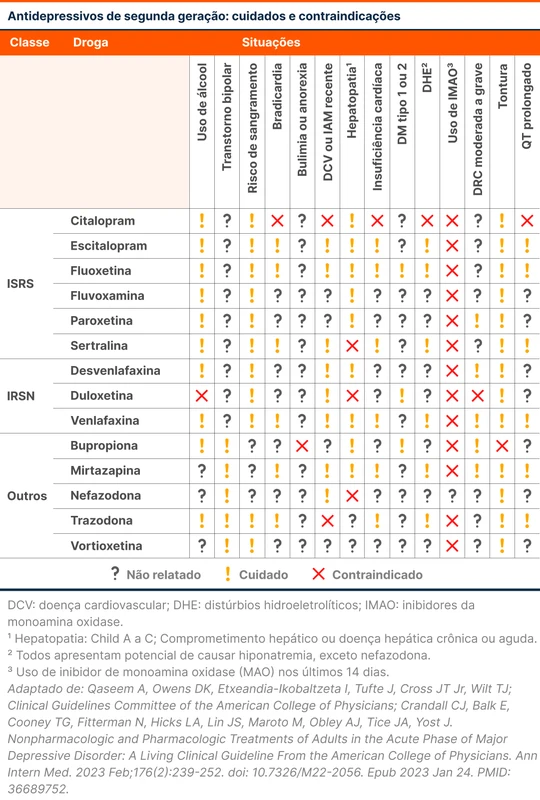
Delirium é uma síndrome com várias causas e manifestações. Os exames complementares que fazem parte da investigação do delirium não são consensuais. O Journal of the American Geriatric Society publicou um trabalho que tenta responder como a tomografia de crânio pode ajudar no esclarecimento das causas de alteração do estado mental ou delirium [1]. Este tópico revisa o diagnóstico e a investigação de delirium e traz os resultados do estudo.
O que é e quais são as causas de delirium?
Delirium é um conjunto de sinais e sintomas que indicam um estado confusional agudo. A evolução é aguda e flutuante e as principais manifestações são alteração na atenção e no nível de consciência [2].
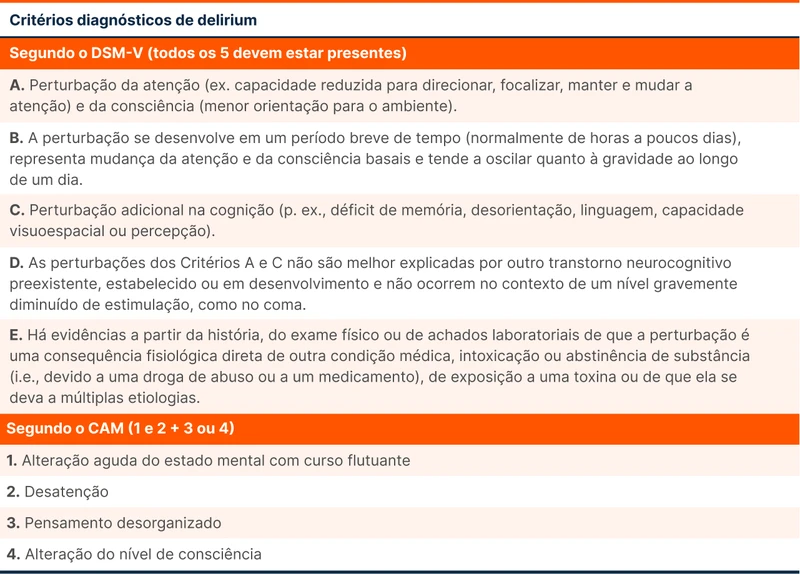
A definição dos quadros de alteração mental não é clara, o que dificulta a interpretação dos resultados de estudos e o diagnóstico de delirium. Atualmente, os critérios diagnósticos de delirium mais utilizados são os do Confusion Assessment Method (CAM) e do Manual de Diagnóstico e Estatístico de Transtornos Mentais 5ª edição (DSM-V), detalhados na tabela 1 [3]. A padronização da definição de delirium permite que esse grupo de pacientes seja identificado de maneira mais homogênea.
A determinação da causa do delirium é necessária para o tratamento adequado. A investigação pode partir da identificação dos fatores de risco. Um paciente com delirium pode apresentar fatores predisponentes (fatores de risco crônicos) e fatores precipitantes (fatores de risco novos).
Em janeiro de 2023 o Journal of the American Medical Association (JAMA) publicou uma revisão sistemática com mais de 300 estudos em pacientes com delirium para identificar fatores predisponentes e precipitantes [4]. Foram encontrados 33 fatores predisponentes e 112 precipitantes. É possível que alguns fatores citados não tenham papel na causa do delirium, mas ocorram apenas em associação a delirium e sejam consequências de fatores causais verdadeiros.
Os fatores predisponentes mais comuns incluem idade avançada, demência ou alterações cognitivas. Os fatores precipitantes foram agrupados em 8 categorias:
- Fatores cirúrgicos;
- Farmacológicos;
- Iatrogênicos e ambientais;
- Trauma;
- Doenças sistêmicas;
- Alterações metabólicas;
- Alterações de biomarcadores;
- Alterações de neurotransmissores séricos ou liquóricos.

O mnemônico DELIRIUM ajuda a organizar a lista de causas (tabela 2).
Quais exames laboratoriais devem ser solicitados na investigação de delirium?
Não há estudos que claramente indiquem quando e quais exames devem ser solicitados para pacientes com delirium. Uma das explicações para essa indefinição é a existência de muitos fatores causais possíveis, frequentemente atuando em conjunto para precipitação do quadro.
Outra dificuldade é a diversidade de apresentações. Muitas vezes o paciente em delirium não é capaz de expressar seus sintomas e o exame físico é dificultado pela alteração do nível de consciência. Dessa forma, os exames laboratoriais são solicitados na ausência de hipóteses clínicas, embasados exclusivamente em dados epidemiológicos - considerando características como a idade, comorbidades e o ambiente em que o paciente está (unidade de terapia intensiva, pós operatório, domicílio). Esta estratégia diminui a acurácia dos testes complementares.
O laboratório básico da investigação do delirium costuma incluir hemograma, marcadores inflamatórios como VHS e PCR, eletrólitos, especialmente o sódio, glicemia, análise de urina e funções renal e hepática.
Outros exames podem ser indicados, como função tireoidiana e toxicológico. Gasometria arterial pode ajudar quando há indícios de sepse ou acidose metabólica. Nos casos de suspeita de infecção, exames de urina e imagem do tórax podem ser solicitados.
A punção lombar (PL) é recomendada nos pacientes em que há suspeita de meningite ou hemorragia subaracnoide. Um estudo retrospectivo identificou que, em idosos hospitalizados com alteração do estado mental e febre, apenas 1 de 81 pacientes puncionados tinha meningite bacteriana [5]. Em casos de delirium persistente ou inesperado (em pacientes jovens), a PL ganha importância [2].
O eletroencefalograma (EEG) deve ser reservado para os casos de delirium que não melhoram ou que não têm a causa identificada após os primeiros exames. Um EEG sem alterações torna o diagnóstico de delirium altamente improvável. Para investigação da causa, é útil no diagnóstico de quadros epilépticos. Cerca de 20% dos pacientes com delirium têm potenciais epilépticos, mas não é claro o papel desses eventos na doença. A frequência do estado epiléptico não convulsivo chega a 14-28% em alguns estudos [6].
É importante solicitar tomografia de crânio para pacientes com delirium?
A revisão sistemática publicada no Journal of the American Geriatric Society tentou definir o rendimento de tomografias de crânio (TC) no delirium [1]. Foram incluídos 46 estudos observacionais de pacientes com delirium ou alteração do estado mental, excluindo pacientes com trauma ou quedas. Apenas quatro trabalhos tinham pacientes diagnosticados com delirium, enquanto os outros envolviam pacientes com quadros heterogêneos incluindo alteração do estado mental, déficits não focais, convulsões, síncope, cefaleia, vertigem e déficits neurológicos focais. Os diagnósticos de delirium e estado mental alterado foram feitos na maioria das vezes sem uma ferramenta padronizada. Oitenta por cento dos estudos foram em pronto-socorro/internação e o restante em UTI.
Foi considerado positivo o achado tomográfico de alterações agudas ou subagudas que justificassem o quadro neurológico. O estudo identificou que o rendimento da TC foi de 12,9% para pacientes do pronto-socorro/internados (intervalo de confiança 95%: 10,2% - 15,9%) e 17,4% em UTI (intervalo de confiança 95%: 10% - 26,3%). Houve bastante heterogeneidade nos achados. Na amostra de pacientes com delirium ou alteração do estado mental, 1 a cada 5 tomografias foi positiva no pronto-socorro/internação e 1 a cada 8 foi positiva na UTI.
A revisão apontou queda do rendimento nas solicitações das tomografias nos estudos após os anos 2000. Uma explicação sugerida para esse achado é a solicitação de TC em excesso, especialmente para pacientes com menor probabilidade pré teste de alterações.
O trabalho sugere que a principal característica que aumenta o rendimento da solicitação de tomografia nesses pacientes é a presença de sinal neurológico focal. Foram excluídas alterações crônicas na tomografia, como as sugestivas de quadros demenciais, que poderiam ter algum valor para explicar a clínica dos pacientes. Os autores concluem que são necessários trabalhos para criação e validação de ferramentas de predição clínica para otimizar as solicitações de TC nesse contexto.