Tromboembolismo Venoso em Pacientes com DPOC Exacerbada
Pacientes com doença pulmonar obstrutiva crônica (DPOC) apresentam risco até duas vezes maior para eventos trombóticos. Os sintomas de tromboembolismo pulmonar podem ser difíceis de distinguir de um episódio de exacerbação de DPOC. Um estudo publicado no International Journal of Chronic Obstructive Pulmonary Disease avaliou a prevalência de eventos tromboembólicos em pacientes admitidos com o diagnóstico de DPOC exacerbada [1]. Este tópico revisa o tema e os achados do estudo.
Diagnósticos diferenciais de DPOC exacerbada
O Global Initiative for Chronic Obstructive Lung Disease (GOLD) de 2023 define exacerbação como uma piora da dispneia e/ou da tosse e secreção que ocorre no período de menos de 14 dias [2].
Uma exacerbação de DPOC é diferente de pneumonia. Na pneumonia, o exame de imagem do pulmão mostra uma nova opacidade ou infiltrado, o que não entra na definição de exacerbação. Assim, a suspeita de exacerbação leva a uma imagem do tórax para avaliar a presença de pneumonia.
As exacerbações de DPOC podem ter causas infecciosas ou não infecciosas. Até 30% dos episódios de exacerbação não tem uma causa definida [3, 4]. Os vírus respiratórios são a principal causa infecciosa de exacerbação. Exposição a poluentes e má aderência medicamentosa são exemplos de causas não infecciosas de exacerbações. Esses fatores contribuem com a piora da dispneia (principal sintoma na exacerbação), acompanhada de aumento e/ou purulência do escarro, tosse e sibilos.
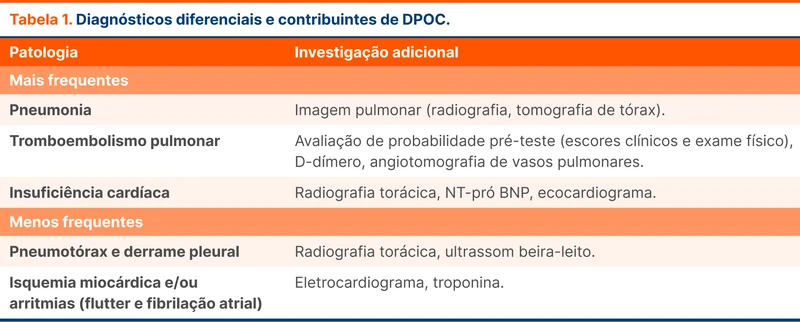
Pacientes com DPOC têm risco aumentado para eventos agudos, como descompensação de insuficiência cardíaca, pneumonia e tromboembolismo pulmonar (TEP). Essas condições podem mimetizar ou até agravar um quadro de exacerbação. O GOLD de 2023 reforça a necessidade de alta suspeição clínica de diagnósticos diferenciais na avaliação de uma exacerbação [2]. Essa suspeita é especialmente importante quando há piora de dispneia sem os outros sinais clássicos de exacerbação (aumento do volume secreção e purulência do escarro) e na ausência de melhora com a terapia inicial. A tabela 1 resume os principais confundidores e contribuintes durante a avaliação de um episódio de DPOC exacerbada.
Risco trombótico do paciente com DPOC exacerbada
Pacientes com DPOC apresentam risco até duas vezes maior para eventos trombóticos em relação à população geral. No paciente com DPOC exacerbada, TEP é o evento trombótico mais prevalente. Isso é diferente da população geral, em que o evento mais comum é a trombose venosa profunda (TVP). Mesmo quando controlada, a DPOC é considerada fator de risco independente para TEP. Na exacerbação aguda, o risco de eventos tromboembólicos venosos pode ser ainda mais elevado [5].
Tanto o GOLD como o American College of Chest Physicians (ACCP) recomendam a instituição de tromboprofilaxia medicamentosa para todo paciente internado com exacerbação de DPOC [6].
Escores de probabilidade clínica para TEP como os escores de Wells e Genebra não foram validados em pacientes com DPOC. No escore de Wells, por exemplo, a variável subjetiva “diagnóstico alternativo mais provável que TEP” pode ser de difícil avaliação durante um episódio de exacerbação aguda.
Resultados do estudo
Esse estudo multicêntrico de coorte prospectiva realizado na China avaliou 1580 pacientes admitidos com o diagnóstico de DPOC exacerbada [1]. Pacientes com contraindicação ao contraste, neoplasia ativa ou uso de anticoagulantes foram excluídos. Todos os participantes foram submetidos ao rastreio de eventos trombóticos com angiotomografia de artéria pulmonar (protocolo TEP) e USG doppler venoso de membros inferiores. Também foram registrados resultados dos escores de Wells e Genebra modificado nas primeiras 24 horas, bem como exames laboratoriais como D-Dímero, BNP ou NT-pró BNP, gasometria arterial e coagulograma [7, 8].
O evento trombótico mais prevalente foi o TEP, com 16,8% de prevalência no momento da admissão, enquanto a prevalência de TVP foi 13,1%. No total, a prevalência de pacientes com algum evento trombótico venoso foi de 24,5%.
O estudo apresenta alguns dados relevantes:
- A presença de escarro purulento esteve menos associado com trombose venosa;
- Histórico de trombose prévia, taquipneia, achados de cor pulmonale e aumento de biomarcadores (D-Dímero, BNP e NT-pró BNP) foram fatores independentes associados com eventos trombóticos;
- A mortalidade em um ano de seguimento e o tempo de hospitalização foram maiores em pacientes com eventos trombóticos;
Estratificando pelos critérios de Wells, foi diagnosticado TEP em 7,4% dos pacientes com probabilidade baixa, 38,4% dos pacientes com probabilidade moderada e 73,7% dos pacientes com alta probabilidade. A prevalência de TEP encontrada no trabalho é maior do que a descrita previamente nos estudos de validação dos critérios de Wells. Esse achado reforça a importância de utilizar esta ferramenta com cautela, especialmente nos pacientes estratificados com baixa probabilidade [9].
Este estudo encontrou taxas relevantes de prevalência de tromboses venosas em pacientes com DPOC exacerbada, em concordância com dados de uma metanálise recente [10]. Estudos prévios não demonstraram taxas tão elevadas, porém variaram muito em critérios de inclusão e na forma de rastreio realizada.
Estes achados reforçam a necessidade de uma alta suspeição clínica e postura ativa no diagnóstico de eventos trombóticos em pacientes com DPOC exacerbada, principalmente em casos de apresentações atípicas. Os sintomas similares de DPOC exacerbada e TEP podem atrasar o diagnóstico e piorar os desfechos. Não é possível extrapolar estes dados para pacientes ambulatoriais.