Betabloqueador Após Infarto Agudo do Miocárdio
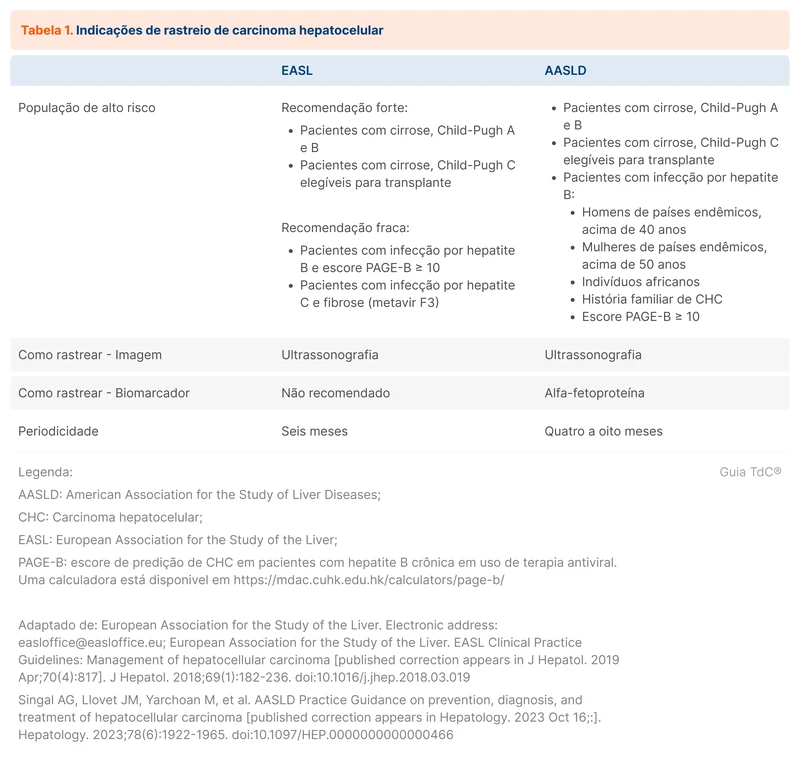
A prescrição de betabloqueadores após infarto agudo do miocárdio (IAM) é uma prática baseada em evidências da década de 80 de diminuição de mortalidade. O ensaio clínico randomizado REDUCE-AMI, publicado em abril de 2024 no New England Journal of Medicine [1], avaliou o uso de betabloqueadores no pós-infarto em pacientes com fração de ejeção preservada. Esse tópico traz os resultados do estudo e discute o tema.
Ecocardiograma no infarto agudo do miocárdio
O ecocardiograma transtorácico é o método de escolha para avaliação da função cardíaca após um IAM. O exame avalia a função ventricular, sinais de isquemia e localiza as paredes com déficit de contratilidade, inferindo a coronária afetada. Também identifica complicações pós-infarto como trombos intracavitários, ruptura de musculatura papilar, de parede ventricular e septo [2]. A fração de ejeção do ventrículo esquerdo (FE) é considerada pela diretriz de IAM da American College of Cardiology/American Heart Association (ACC/AHA) como um dos melhores preditores de sobrevida pós-infarto [3].
Um valor de FE ≤ 40% caracteriza uma FE reduzida. Esses pacientes têm mortalidade aumentada e se beneficiam de drogas específicas que trazem melhora na sobrevida. Uma FE entre 41 e 49% é classificada como levemente reduzida. Esses pacientes em geral são tratados de maneira similar àqueles com FE reduzida. Uma FE ≥ 50% é considerada preservada.
Um ecocardiograma precoce pode identificar FE reduzida por "miocárdio atordoado", uma disfunção pós isquêmica transitória que melhora após o tratamento de reperfusão [4]. O estudo US HEART identificou que 22% dos pacientes infartados com supradesnivelamento de ST e com FE reduzida recuperaram de maneira completa a função ventricular, principalmente nos primeiros 14 dias após a reperfusão [5].
Não há consenso sobre o momento em que o ecocardiograma deve ser realizado após um infarto. A diretriz de IAM da European Society of Cardiology (ESC) recomenda que seja feito antes da alta hospitalar e, caso seja identificada FE ≤ 40%, deve ser repetido em seis a doze semanas após [6]. Realizar um ecocardiograma entre dois a sete dias após o infarto e repeti-lo em algumas semanas pode auxiliar no prognóstico desses pacientes [7].
Betabloqueadores para pacientes com fração de ejeção reduzida (≤ 40%) pós-infarto
Estudos demonstram redução de mortalidade, morbidade e sintomas com o uso de betabloqueador na insuficiência cardíaca (IC) com FE reduzida. Pacientes assintomáticos com FE ≤ 40% são considerados pela ACC/AHA como pré-insuficiência cardíaca (estágio B). Existem evidências para uso de inibidores da enzima conversora de angiotensina (iECA), bloqueadores do receptor da angiotensina (BRA) e betabloqueadores para pacientes com FE reduzida, mesmo assintomáticos, para redução de mortalidade. O benefício do betabloqueador ocorre especialmente nos pacientes com IAM prévio [8]. Dessa forma, nos pacientes que infartaram e evoluíram com FE ≤ 40%, a medicação está indicada mesmo se não existirem sintomas de IC [8, 9].
O tópico sobre semaglutida na insuficiência cardíaca de fração de ejeção preservada traz a definição universal de IC. Mais detalhes sobre a diretriz de IC de 2022 da ACC/AHA estão no tópico sobre a diretriz.
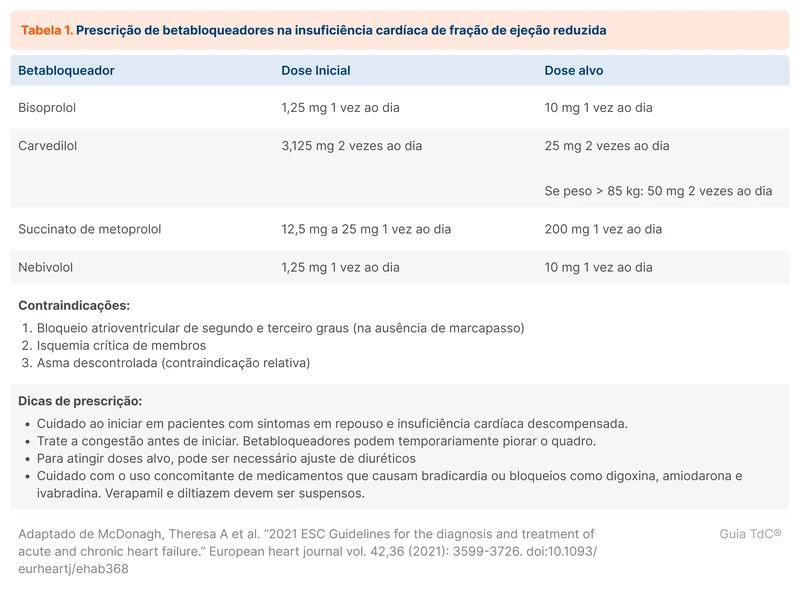
Quatro betabloqueadores são considerados de primeira linha no tratamento da IC com FE reduzida por terem ensaios clínicos randomizados com evidência de benefício:
A tabela 1 traz informações sobre a prescrição de betabloqueadores [9].
Betabloqueadores para pacientes com fração de ejeção preservada (≥ 50%) pós-infarto
A evidência para o uso de betabloqueadores em pacientes com IAM e FE > 40% é menos estabelecida. O benefício de redução da mortalidade após IAM foi encontrada em estudos antigos, feitos em uma época em que o tratamento era menos eficaz. A maioria dos trabalhos incluiu pacientes com supradesnivelamento de ST em uma época pré-trombólise e não estratificou os pacientes por FE [14-17].
Estudos observacionais mais recentes foram discordantes e novos ensaios clínicos randomizados estão sendo realizados [18-20]. O estudo japonês CAPITAL-RCT incluiu 800 pacientes com IAM com supradesnivelamento de ST e intervenção coronariana percutânea (ICP) bem sucedida e FE preservada e não houve diferença entre o grupo carvedilol e placebo após três anos de acompanhamento [21].
Apesar da dúvida do benefício, as últimas diretrizes americana e europeia recomendam o uso dos betabloqueadores para todos os pacientes que infartaram, desde que não tenham contraindicações [3, 6, 22]. Existe dúvida se o benefício da medicação pode estar restrito apenas ao primeiro ano de uso [23].
REDUCE-AMI: ausência de benefício sobre betabloqueadores pós-infarto
O REDUCE-AMI foi um ensaio clínico randomizado aberto multicêntrico que selecionou pacientes que infartaram e fizeram tratamento com ICP. Os pacientes tinham FE ≥ 50% após um a sete dias do infarto. Os pacientes do grupo intervenção utilizaram metoprolol ou bisoprolol e o grupo controle foi orientado a não utilizar betabloqueadores. O desfecho primário foi composto de morte e novo infarto.
De setembro de 2017 a maio de 2023, mais de 5000 pacientes foram incluídos com mediana de idade de 65 anos, sendo 80% homens. No momento da entrada no pronto-socorro, 35% tinham supradesnivelamento de ST e 11% já usavam betabloqueadores. A maioria dos pacientes tinha lesão de uma coronária apenas e 16% tinham lesão de tronco ou das três coronárias. O tratamento com ICP foi feito em 95% dos pacientes e revascularização miocárdica cirúrgica em 4%. A população do estudo representava uma população em geral de baixo risco para novos eventos cardíacos.
Em um acompanhamento médio de três anos e meio, o uso de betabloqueadores após um IAM em pacientes com FE ≥ 50% não mudou o desfecho primário composto de morte e novo infarto. Não houve impacto em desfechos secundários como morte por qualquer causa, morte por causa cardiovascular, novo IAM, hospitalização por fibrilação atrial e hospitalização por IC. Houve incidência semelhante nos desfechos de segurança. Esses achados foram encontrados em todos os subgrupos analisados, inclusive nos pacientes com IAM prévio e não houve diferença para pacientes com ou sem supradesnivelamento de ST.
A taxa de eventos de interesse (morte e IAM) na população foi menor do que a prevista, reduzindo o poder estatístico para detectar pequenos benefícios ou malefícios entre os grupos. No grupo controle, 10% tiveram alta com betabloqueador e 14% estavam utilizando o medicamento após um ano de acompanhamento. Não é possível descartar que um possível benefício tenha sido mascarado, levando ao resultado negativo do trabalho.
Novos estudos em pacientes com FE preservada estão em andamento, como o REBOOT-CNIC, BETAMI e DANBLOCK e talvez tragam novas conclusões sobre o tema.